
 .
.分析 A是有机羧酸盐HCOONa,B、C、D是常见化合物; A、B、C、D焰色反应呈黄色,水溶液均呈碱性,则可推知化合物A、B、C、D均为含有Na元素的碱或强碱弱酸盐,B的碱性最强,则B为NaOH;X、Y是最常见的氧化物且与人体、生命息息相关,它们的晶体类型相同,则X、Y应为H2O和CO2中的一种,由D受热分解得到Y、C和X;B与D反应生成C和X,可推知D为NaHCO3,C为Na2CO3,④D(s) $\frac{\underline{\;△\;}}{\;}$ C+X+Y即2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O;③B+D═C+X 即 NaHCO3+NaOH=Na2CO3+H2O,故X为H2O,Y为CO2,A是有机羧酸盐,反应①A(s)+B(s)$\stackrel{△}{→}$ C(s)+H2↑,C为Na2CO3,B为NaOH,则A为HCOONa,反应②为NaHCO3+H2=HCOONa+H2O;
由此可解答问题;
(1)C为碳酸钠;
(2)为氢氧化钠属于离子化合物;
(3)反应是可逆的过程无污染、安全;
(4)上述分析可知C为碳酸钠属于盐,是离子化合物,结构中含有共价键和离子键;
(5)Y的晶体为二氧化碳晶体,是分子晶体,固体融化破坏的是分子间作用力;
(6)X为水,形成的晶体为分子晶体,晶体中含有氢键,形成的是正四面体结构空间网状结构,熔沸点高;
(7)反应①是甲酸钠和氢氧化钠固体加热反应生成氢气和碳酸钠;
(8)在C的饱和溶液中不断通Y析出D的反应为二氧化碳气体通入碳酸钠饱和溶液中生成碳酸氢钠晶体析出;
(9)泡沫灭火器灭火原理是碳酸氢钠恒容硫酸铝水溶液中发生双水解反应生成氢氧化铝沉淀和二氧化碳气体;
解答 解:依据题干信息分析推断,A是有机羧酸盐HCOONa,B、C、D是常见化合物; A、B、C、D焰色反应呈黄色,水溶液均呈碱性,则可推知化合物A、B、C、D均为含有Na元素的碱或强碱弱酸盐,B的碱性最强,则B为NaOH;X、Y是最常见的氧化物且与人体、生命息息相关,它们的晶体类型相同,则X、Y应为H2O和CO2中的一种,由D受热分解得到Y、C和X;B与D反应生成C和X,可推知D为NaHCO3,C为Na2CO3,④D(s) $\frac{\underline{\;△\;}}{\;}$ C+X+Y即2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O;③B+D═C+X 即 NaHCO3+NaOH=Na2CO3+H2O,故X为H2O,Y为CO2,A是有机羧酸盐,反应①A(s)+B(s)$\stackrel{△}{→}$ C(s)+H2↑,C为Na2CO3,B为NaOH,则A为HCOONa,反应②为NaHCO3+H2=HCOONa+H2O;
(1)上述分析可知C的名称是碳酸钠;
故答案为:碳酸钠;
(2)B为氢氧化钠,属于离子化合物,钠离子和氢氧根离子构成的离子化合物氢氧化钠的电子式是: ;
;
故答案为: ;
;
(3)可逆反应会在一定条件下发生破坏移动储氢或释氢,上述②储氢方法的二个最明显的优点是无污染环保,安全;
故答案为:环保;安全;
(4)上述分析可知C为碳酸钠属于盐,是由钠离子和碳酸根离子构成的离子化合物,结构中含有共价键和离子键;
故答案为:离子;离子;共价;
(5)Y为二氧化碳,Y的晶体为二氧化碳晶体,是分子晶体,晶体熔化时仅克服分子间作用力;
故答案为:分子间作用;
(6)X为水,形成的晶体为分子晶体,晶体中水分子和水分子间形成的分子间作用力含有氢键,晶体形成的晶胞是正四面体结构的空间网状结构,所以熔沸点高;
故答案为:氢;正四面;高;
(7)反应①是甲酸钠和氢氧化钠固体加热反应生成氢气和碳酸钠,反应的化学方程式为:HCOONa+NaOH $\frac{\underline{\;△\;}}{\;}$Na2CO3+H2↑;
故答案为:HCOONa+NaOH $\frac{\underline{\;△\;}}{\;}$Na2CO3+H2↑;
(8)在C的饱和溶液中不断通Y析出D的反应为二氧化碳气体通入碳酸钠饱和溶液中生成碳酸氢钠晶体析出,反应的离子方程式为:2Na++CO32-+H2O+CO2═2NaHCO3↓;
故答案为:2Na++CO32-+H2O+CO2═2NaHCO3↓;
(9)泡沫灭火器灭火原理是碳酸氢钠恒容硫酸铝水溶液中发生双水解反应生成氢氧化铝沉淀和二氧化碳气体,反应的离子方程式为:3HCO3-+Al3+═Al(OH)3↓+3CO2↑;
故答案为:3HCO3-+Al3+═Al(OH)3↓+3CO2↑.
点评 本题考查了物质性质和变化的分析判断,主要是物质结构、物质性质的分析应用,掌握反应特征和反应产物是解题关键,题目难度中等.


 励耘书业暑假衔接宁波出版社系列答案
励耘书业暑假衔接宁波出版社系列答案科目:高中化学 来源: 题型:选择题
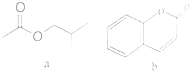
| A. | a属于不饱和烃 | |
| B. | a、b含有的官能团种类相同 | |
| C. | 1molb最多能和4molH2反应 | |
| D. | 等物质的量的a、b最多消耗NaOH的量相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | X、Y元素能与氢形成分子式为H2XY2、H4X2Y2等弱酸 | |
| B. | 化合物ZY2中只含有离子键 | |
| C. | 工业上可用X单质置换ZY得到Z单质 | |
| D. | Y的氢化物的沸点比其下一周期的同族元素的氢化物的沸点低 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乳酸薄荷醇酯(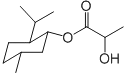 )仅能发生水解、氧化、消去反应 )仅能发生水解、氧化、消去反应 | |
| B. | 乙醛和丙烯醛(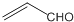 )不是同系物,它们与氢气充分反应后的产物是同系物 )不是同系物,它们与氢气充分反应后的产物是同系物 | |
| C. | 乙烯、聚氯乙烯和苯分子中均含有碳碳双键 | |
| D. | CH3COOCH2CH3与CH3CH2COOCH3互为同分异构体,核磁共振氢谱显示两者均有三种不同的氢原子且三种氢原子的比例相同,故不能用核磁共振氢谱鉴别 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2CO3固体(NaHCO3) 加热 | B. | I2(沙子) 加热 | ||
| C. | Na2O2(Na2O) 氧气中加热 | D. | Cl2(HCl) 通过NaOH溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ④⑤ | B. | ④⑤⑦ | C. | ③④⑤ | D. | ③④⑤⑦ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com