

分析 ①根据仪器的形状来分析;
②A、由图可知,所配溶液的体积为100mL,根据n=$\frac{m}{M}$计算碳酸钠的物质的量;
B、由图可知操作2是移液,用玻璃棒引流;
C、操作4是定容,应滴加水至溶液凹液面的最低点与刻度线平齐;
D、定容摇匀后发现液面低于刻度线,少量溶液残留在瓶塞与瓶口之间,再加水至液面与刻度线平齐,导致所配溶液的体积偏大.
解答 解:①操作2中容器的名称是100mL容量瓶,故答案为:100mL容量瓶;
②A、由图可知,所配溶液的体积为100mL,10.6g碳酸钠的物质的量为$\frac{10.6g}{106g/mol}$=0.1mol,故A正确;
B、由图可知操作2是将溶解得到的碳酸钠溶液移入容量瓶,玻璃棒的作用是引流,故B正确;
C、操作4是定容,应滴加水至溶液凹液面的最低点与刻度线平齐,故C正确;
D、定容摇匀后发现液面低于刻度线,少量溶液残留在瓶塞与瓶口之间,再加水至液面与刻度线平齐,导致所配溶液的体积偏大,所配溶液的浓度偏小,故D错误.
故选D.
点评 本题考查了一定物质的量浓度溶液的配制过程中的计算和误差分析,属于基础型题目,难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 氧气 | B. | 氮气 | C. | C2H4 | D. | NO |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
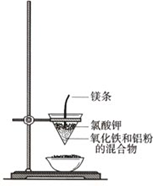 铁和铝是两种重要的金属.请回答:
铁和铝是两种重要的金属.请回答:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 理由 | 结论 |
| A | 碱性:Ba(OH)2>Mg(OH)2 | 金属性:Ba>Mg |
| B | 相同物质的量的原子失去电子的数目:Al>Na | 还原性:Al>Na |
| C | HX酸性比HY强 | 非金属性:X>Y |
| D | 相同物质的量得到电子的数目:稀硝酸>浓硝酸 | 氧化性:稀硝酸>浓硝酸 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③⑤⑥ | B. | ①②⑤⑥ | C. | ②③④⑥ | D. | ③④⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com