
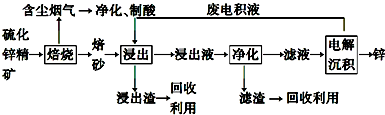
分析 (1)焙烧中硫化锌与氧气在高温下反应生成氧化锌和二氧化硫,据此写出反应的化学方程式;
(2)①ZnS在氧气燃烧发生氧化还原反应生成产物出来氧化锌外还有硫的氧化物,可转换为硫酸,用于后续的浸出操作;
②锌的活泼性强于铁,能够与二价铁离子反应生成铁;
③依据题意“氧压酸浸”的全湿法流程,既省略了易导致空气污染的焙烧过程,又可获得一种有工业价值的非金属单质,可知反应物中含有H+和O2,可以获得非金属单质S,据此写出方程式;
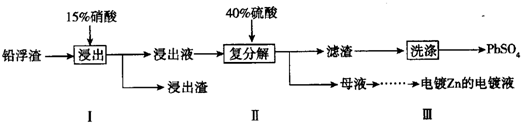
(3)①根据题给信息硝酸把铅氧化成Pb2+,硝酸被还原成NO,据此写出方程式;
②铅浮渣中含银,银也和硝酸反应;硫酸钙微溶,易沉淀在PbSO4表面,所以需用Pb(NO3)2溶液多次洗涤,除去CaSO4;
③Pb(NO3)2溶液加硫酸后生成硫酸铅沉淀和硝酸,过滤得滤液含硝酸;铁棒上镀锌,镀层金属作阳极,锌作阳极;
(4)正极得电子发生还原反应,根据总反应书写电极方程式.
解答 解:(1)由题中信息可知,闪锌矿(主要成分是ZnS)通过浮选焙烧使它转化为氧化锌,反应的化学方程式为:2ZnS+3O2$\frac{\underline{\;高温\;}}{\;}$2ZnO+2SO2;
故答案为:2ZnS+3O2$\frac{\underline{\;高温\;}}{\;}$2ZnO+2SO2;
(2)①ZnS在氧气燃烧发生氧化还原反应生成产物出来氧化锌外还有硫的氧化物,可转换为硫酸,用于后续的浸出操作;
故答案为:浸出;
②该含锌矿中还含有FeS等杂质,浸出操作后转化为亚铁离子,可加入锌粉出去亚铁离子,离子方程式:Zn+Fe2+=Zn2++Fe;
故答案为:置换出Fe等,以达到净化的目的;
③“氧压酸浸”法顾名思义,可知反应物中含有H+和O2,可以获得非金属单质S,写出化学方程式为:2ZnS+4H++O2=2Zn2++2S↓+2H2O,
故答案为:2ZnS+4H++O2=2Zn2++2S↓+2H2O;
(3)①根据题给信息硝酸把铅氧化成Pb2+,硝酸被还原成NO,故反应方程式为3Pb+8HNO3=3Pb(NO3)2+2NO↑+4H2O;
故答案为:3Pb+8HNO3=3Pb(NO3)2+2NO↑+4H2O;
②若硝酸过量,则过量的硝酸会和银反应生成硝酸银,产品中会有杂质,所以步骤I需控制硝酸的用量并使Pb稍有剩余,其目的是防止Ag被溶解进入溶液;硫酸钙微溶,易沉淀在PbSO4表面,所以需用Pb(NO3)2溶液多次洗涤,除去CaSO4,
故答案为:防止Ag被溶解进入溶液(或使Ag留在浸出渣中);除去附着在硫酸铅表面的微溶物硫酸钙;
③Pb(NO3)2溶液加硫酸后生成硫酸铅沉淀和硝酸,所以母液可循环利用于步骤I,其溶质主要是HNO3,铁棒上镀锌,镀层金属作阳极,锌作阳极,
故答案为:HNO3;Zn或锌;
(4)正极得电子发生还原反应,电极方程式为:Ag2O+H2O+2e-═2Ag+2OH-,
故答案为:Ag2O+H2O+2e-═2Ag+2OH-.
点评 本题为工艺流程题,通过锌的炼制、金属的冶炼原理、电解原理及其应用,考查了化学方程式、离子方程式的书写及计算,物质分离提纯的方法,明确工艺流程及各种物质的性质是解题关键,题目难度中等.


科目:高中化学 来源: 题型:解答题
 1,2-二溴乙烷是常用的有机合成中间体,某小组用如图装置合成1,2-二溴乙烷.
1,2-二溴乙烷是常用的有机合成中间体,某小组用如图装置合成1,2-二溴乙烷.| 沸点/℃ | 密度/(g•cm-3) | 水中溶解性 | |
| 1,2二溴乙烷 | 131.4 | 2.18 | 微溶 |
| 溴 | 58.8 | 3.12 | 微溶 |
| 乙醇 | 78.5 | 0.79 | 溶 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 根据以上信息,可推断CH3COOH为弱电解质 | |
| B. | 加水稀释过程中,c(H+)•c(OH-) 的值增大 | |
| C. | 加入NaOH固体可抑制 CHCOO-的水解 | |
| D. | 同pH的CH3COONa溶液和NaOH溶液,由水电离出的c(H+) 前者大 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 离子 | K+ | Na+ | NH4+ | SO42- | NO3- | Cl- |
| 浓度/mol•L-1 | 4×10-6 | 6×10-6 | 2×10-5 | 4×10-5 | 3×10-5 | 2×10-5 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1molCl2和足量的铁加热条件下反应,转移电子数一定为3NA | |
| B. | 28g乙烯和丙烯的混合物中含有双键数目小于NA | |
| C. | 常温下,PH=13的Ba(OH)2 溶液,0.1L,含OH-,0.02NA | |
| D. | 1 L 1 mol/L的甲醇水溶液中含有氢原子总数为4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
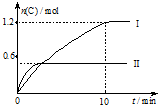 在2L的恒容密闭容器中充入A(g)和B(g),发生反应A(g)+B(g)?2C(g)+D(s)△H=a kJ•mol-1
在2L的恒容密闭容器中充入A(g)和B(g),发生反应A(g)+B(g)?2C(g)+D(s)△H=a kJ•mol-1| 实验序号 | 温度 | 起始物质的量 | |
| A | B | ||
| Ⅰ | 600℃ | 1mol | 3mol |
| Ⅱ | 800℃ | 1.5mol | 0.5mol |
| A. | 实验 I中,10 min内平均反应速率v(B)=0.06 mol•L-1•min-1 | |
| B. | 上述方程式中,a<0 | |
| C. | 600℃时,该反应的平衡常数是0.45 | |
| D. | 向实验Ⅱ的平衡体系中再充入0.5 mol A和1.5 molB,A的转化率增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 室温下向1 L pH=1的醋酸溶液中加水,所得溶液的OH-数目大于0.1NA | |
| B. | 60g乙酸与足量乙醇发生酯化反应,充分反应后乙酸断裂的C-O键数目为NA | |
| C. | 已知C2H4(g)+H2(g)=C2H6(g)△H=-137.0 kI/mol,乙烯与H2加成时放出68.5 kJ热量,则 反应过程中被破坏的碳原子之间共用电子对数目为NA | |
| D. | 4.6gSO2、NO2混合气体中含有中子数为2.3 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 温度升高,该反应反应速率加快,平衡常数增大 | |
| B. | 题目所述的某时刻正、逆反应速率的大小为V(正)>V(逆) | |
| C. | 经10min反应达到平衡,则该时间内反应速率v(A)为0.064mol/(L•min) | |
| D. | 平衡时,再加入与起始等量的A,达新平衡后A的转化率增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
| 元素 | A | B | C | D | E |
| 相关 信息 | A元素原子核外有3个电子层,最外层有3个电子. | 与元素C可形成离子个数比 为2:1和1:1的化合物 | C元素的原子K、L层电子数之和比L、M层电子数之和多1个电子 | D元素可形成两种氧化物,其中一种是形成酸雨的主要成分 | 其单质是用途最广泛的金属, 人体缺少该元素易患贫血症 |
 、
、 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com