
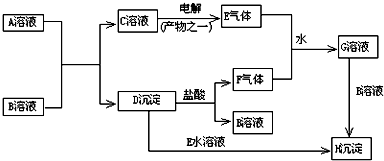
·ÖĪö AµÄŃęÉ«·“Ó¦³Ź»ĘÉ«£¬ŌņAÖŠŗ¬ÓŠÄĘŌŖĖŲ£¬E”¢FĪŖÓŠ“Ģ¼¤ŠŌĘųĪ¶µÄĘųĢ壬µē½āCµÄČÜŅŗµĆµ½ĘųĢåE£¬³ĮµķDÓėŃĪĖį·“Ó¦µĆµ½ĘųĢåF£¬E”¢FŗĶĖ®·“Ӧɜ³ÉG£¬GĪŖĒæĖįŠŌČÜŅŗ£¬ŌņE”¢FĪŖ¶žŃõ»ÆĮņŗĶĀČĘų£¬FŅ²ŹĒŌģ³ÉĖįÓźµÄÖ÷ŅŖ³É·Ö£¬ŌņEĪŖCl2£¬FĪŖSO2£¬GÖŠŗ¬ÓŠHCl”¢H2SO4£¬DÓėEµÄČÜŅŗÉś³ÉH³Įµķ£¬HĪŖ¼ČÄŃČÜÓŚĖ®”¢Ņ²ÄŃČÜÓŚĻ”ĖįµÄ°×É«¹ĢĢ壬ŌņHĪŖBaSO4£¬DĪŖBaSO3£¬BĪŖBaCl2£¬AĪŖNa2SO3£¬CĪŖNaCl£®
½ā“š ½ā£ŗAµÄŃęÉ«·“Ó¦³Ź»ĘÉ«£¬ŌņAÖŠŗ¬ÓŠÄĘŌŖĖŲ£¬E”¢FĪŖÓŠ“Ģ¼¤ŠŌĘųĪ¶µÄĘųĢ壬µē½āCµÄČÜŅŗµĆµ½ĘųĢåE£¬³ĮµķDÓėŃĪĖį·“Ó¦µĆµ½ĘųĢåF£¬E”¢FŗĶĖ®·“Ӧɜ³ÉG£¬GĪŖĒæĖįŠŌČÜŅŗ£¬ŌņE”¢FĪŖ¶žŃõ»ÆĮņŗĶĀČĘų£¬FŅ²ŹĒŌģ³ÉĖįÓźµÄÖ÷ŅŖ³É·Ö£¬ŌņEĪŖCl2£¬FĪŖSO2£¬GÖŠŗ¬ÓŠHCl”¢H2SO4£¬DÓėEµÄČÜŅŗÉś³ÉH³Įµķ£¬HĪŖ¼ČÄŃČÜÓŚĖ®”¢Ņ²ÄŃČÜÓŚĻ”ĖįµÄ°×É«¹ĢĢ壬ŌņHĪŖBaSO4£¬DĪŖBaSO3£¬BĪŖBaCl2£¬AĪŖNa2SO3£¬CĪŖNaCl£®
£Ø1£©ÓÉÉĻŹö·ÖĪöæÉÖŖ£¬AĪŖNa2SO3£¬BĪŖBaCl2£¬
¹Ź“š°øĪŖ£ŗNa2SO3£»BaCl2£»
£Ø2£©¢Ł·“Ó¦C”śEµÄ»Æѧ·½³ĢŹ½ĪŖ£ŗ2NaCl+2H2O$\frac{\underline{\;µē½ā\;}}{\;}$2NaOH+Cl2”ü+H2”ü£¬
¢ŚD+E+H2O”śHµÄ»Æѧ·½³ĢŹ½£©£ŗBaSO3+Cl2+H2O=BaSO4”ż+2HCl£¬
¢ŪE+F+H2O”śGµÄĄė×Ó·½³ĢŹ½ĪŖ£ŗSO2+Cl2+2H2O=SO42-+4H++2Cl-£¬
¹Ź“š°øĪŖ£ŗ2NaCl+2H2O$\frac{\underline{\;µē½ā\;}}{\;}$2NaOH+Cl2”ü+H2”ü£»BaSO3+Cl2+H2O=BaSO4”ż+2HCl£»SO2+Cl2+2H2O=SO42-+4H++2Cl-£»
£Ø3£©µē½āĀČ»ÆÄĘČÜŅŗµĆµ½ĀČĘųŅŌĶāµÄĘųĢåĪŖĒāĘų£¬ĒāĘųČ¼ÉÕČČĪŖ285.8kJ/mol£¬ŌņĒāĘųČ¼ÉÕµÄČČ»Æѧ·½³ĢŹ½£ŗH2£Øg£©+$\frac{1}{2}$O2£Øg£©=H2O £Øl£©”÷H=-285.8kJ/mol£¬
¹Ź“š°øĪŖ£ŗH2£Øg£©+$\frac{1}{2}$O2£Øg£©=H2O £Øl£©”÷H=-285.8kJ/mol£»
£Ø4£©FĪŖSO2£¬½«FĘųĢåĶØČėĘ·ŗģČÜŅŗÖŠµÄĻÖĻóŹĒ£ŗĘ·ŗģČÜŅŗĶŹÉ«£¬ÓÉ“ĖĻÖĻóĖµĆ÷FĘųĢå¾ßÓŠµÄŠŌÖŹŹĒĘư׊Ō£¬
¹Ź“š°øĪŖ£ŗĘ·ŗģČÜŅŗĶŹÉ«£»Ęư׊Ō£®
µćĘĄ ±¾Ģāæ¼²éĪŽ»śĪļµÄĶʶĻ£¬AµÄŃęÉ«·“Ó¦³Ź»ĘÉ«£¬E”¢FĪŖÓŠ“Ģ¼¤ŠŌĘųĪ¶µÄĘųĢ壬GĪŖĒæĖįŠŌČÜŅŗµČŹĒĶʶĻĶ»ĘĘæŚ£¬ŌŁ½įŗĻ×Ŗ»Æ¹ŲĻµ½ųŠŠĶʶĻ£¬¶ŌѧɜµÄĀß¼ĶĘĄķÄÜĮ¦Ģį³ö½ĻøßµÄŅŖĒó£¬ŗÜŗƵŲæ¼²éѧɜµÄĖ¼Ī¬”¢ĶʶĻ”¢·ÖĪöÄÜĮ¦£¬ŹģĮ·ÕĘĪÕŌŖĖŲ»ÆŗĻĪļŠŌÖŹ£¬ĢāÄæÄѶČÖŠµČ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 78 g Na2O2ÖŠ“ęŌŚµÄ¹²¼Ū¼ü×ÜŹżĪŖNA | |
| B£® | 0.1 mol${\;}_{38}^{90}$SrŌ×ÓÖŠŗ¬ÖŠ×ÓŹżĪŖ3.8NA | |
| C£® | ĒāŃõČ¼ĮĻµē³Ųøŗ¼«ĻūŗÄ2.24 LĘųĢåŹ±£¬µēĀ·ÖŠ×ŖŅʵĵē×ÓŹżĪŖ0.1NA | |
| D£® | 0.1 molĀČ»ÆĢśČÜÓŚ1LĖ®ÖŠ£¬ĖłµĆČÜŅŗÖŠFe3+µÄŹżÄæĪŖ0.1NA |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
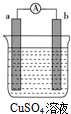 ijŌµē³ŲµÄ×°ÖĆČēĶ¼ĖłŹ¾£¬æ“µ½a¼«ÉĻÓŠŗģÉ«½šŹōĪö³ö£¬»Ų“šĻĀĮŠĪŹĢā£ŗ
ijŌµē³ŲµÄ×°ÖĆČēĶ¼ĖłŹ¾£¬æ“µ½a¼«ÉĻÓŠŗģÉ«½šŹōĪö³ö£¬»Ų“šĻĀĮŠĪŹĢā£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 £®
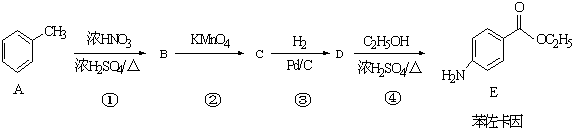
£®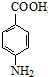 +CH3CH2OH$”ś_{”÷}^{ÅØĮņĖį}$
+CH3CH2OH$”ś_{”÷}^{ÅØĮņĖį}$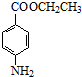 +H2O
+H2O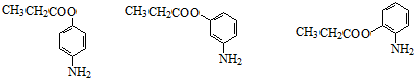 £ØĘäÖŠŅ»ÖÖ£©£ØČĪŠ“Ņ»ÖÖ£©
£ØĘäÖŠŅ»ÖÖ£©£ØČĪŠ“Ņ»ÖÖ£© £©µÄŗĻ³ÉĀ·ĻßĶ¼£ØĘäĖūŌĮĻČĪŃ”£©£®
£©µÄŗĻ³ÉĀ·ĻßĶ¼£ØĘäĖūŌĮĻČĪŃ”£©£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | µē½ā¾«Į¶ĶµÄ¹ż³ĢÖŠ£¬Ćæ×ŖŅĘNAøöµē×ÓŹ±£¬Ńō¼«ČܽāĶµÄÖŹĮæĪŖ32g | |
| B£® | 1 molNa2O2¹ĢĢåÖŠŗ¬Ąė×Ó×ÜŹżĪŖ4NA | |
| C£® | 1molōĒ»łÓė17gNH3Ėłŗ¬µē×ÓŹżÖ®±ČĪŖ9£ŗ10 | |
| D£® | 1molNa2CO3¾§ĢåÖŠŗ¬CO32-Ąė×ÓŹżŠ”ÓŚNA |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
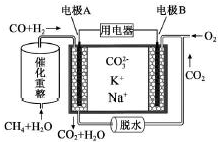
| A£® | Õż¼«²śĪļĪŖCO2 | |
| B£® | øŗ¼«µē¼«·“Ó¦Ź½ĪŖCO-2e-+CO32-ØT2CO2 | |
| C£® | µē³Ų¹¤×÷Ź±£¬CO32-Ļņµē¼«AŅĘ¶Æ | |
| D£® | µē³Ų×Ü·“Ó¦Ź½ĪŖCO+H2+O2ØT2CO2+H2O |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
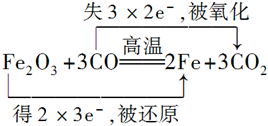 £®
£®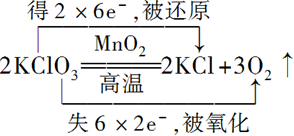 £®
£® £®
£®²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com