
| A. | 乙醛在LiAlH4的作用下生成乙醇,LiAlH4作还原剂 | |
| B. | LiH中两种微粒半径:H->Li+ | |
| C. | 1mol LiAlH4在125℃完全分解,则转移4mol电子 | |
| D. | LiH溶于水的化学反应方程式:LiH+H2O═LiOH+H2↑ |
分析 A.乙醛变化为乙醇的过程是加氢反应,是乙醛被还原发生还原反应;
B.电子层结构相同核电荷数越小半径越大;
C.依据LiAlH4在125℃分解为LiH、H2和Al的化学方程式计算;
D.LiH溶于水发生归中反应生成氢气.
解答 解:A.乙醛变成乙醇得到氢,在有机中得氢去氧是还原,所以氧化剂是乙醛,LiAlH4是还原剂,故A正确;
B.电子层结构相同核电荷数越小半径越大,所以微粒半径:H->Li+,故B正确;
C.LiAlH4中的Li、Al都是主族金属元素,H是非金属元素,故Li为+1价、Al为+3价、H为-1价,受热分解时,根据Al元素的价态变化即可得出1 mol LiAlH4在125℃时完全分解,转移3 mol电子,故C错误;
D.LiH溶于水发生归中反应生成氢气,所以反应的化学方程式为:LiH+H2O═LiOH+H2↑,故D正确;
故选C.
点评 本题考查了氧化还原反应的应用,明确有机反应中氧化剂和还原剂的判断、电子转移数的计算,会结合信息利用知识迁移的方法解决问题.


科目:高中化学 来源: 题型:选择题
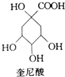 奎尼酸是制备艾滋病新药二咖啡酰奎尼酸的原料,其结构简式如图所示,下列有关奎尼酸的说法中错误的是( )
奎尼酸是制备艾滋病新药二咖啡酰奎尼酸的原料,其结构简式如图所示,下列有关奎尼酸的说法中错误的是( )| A. | 分子式为C7H12O6 | B. | 不能发生加成反应 | ||
| C. | 能与乙醇发生酯化反应 | D. | 1mol奎尼酸最多能消耗6molNaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 工业上利用电解饱和食盐水制氯气:2H++2Cl-$\frac{\underline{\;通电\;}}{\;}$H2↑+Cl2↑ | |
| B. | 将过量二氧化硫气体通入氨水中:SO2+NH3•H2O═HSO${\;}_{3}^{-}$+NH${\;}_{4}^{+}$ | |
| C. | 用碳酸钠溶液浸泡锅炉水垢:CaSO4+CO${\;}_{3}^{2-}$═CaCO3↓+SO${\;}_{3}^{2-}$ | |
| D. | 用稀硝酸洗涤试管内壁的银镜:3Ag+4H++NO${\;}_{3}^{-}$═3Ag++NO↑+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Al2O3$→_{△}^{NaOH(aq)}$NaAlO2(aq)$\stackrel{CO_{2}}{→}$Al(OH)3 | |
| B. | S$\stackrel{O_{2}/点燃}{→}$SO3$\stackrel{H_{2}O}{→}$H2SO4 | |
| C. | Fe2O3$\stackrel{HCl(aq)}{→}$FeCl3(aq)$\stackrel{△}{→}$无水FeCl3 | |
| D. | NH3$\stackrel{O_{2}/催化剂}{→}$NO2$\stackrel{H_{2}O}{→}$HNO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 青砖(含Fe3O4)中的Fe2+可用浓盐酸溶解后,再加入适量高锰酸钾溶液进行检验 | |
| B. | 用0.1000 mol•L-1 NaOH溶液滴定20.00 mL未知浓度盐酸,接近终点时因滴速太快造成NaOH少许过量;此时若加入一定体积该盐酸后,继续用该NaOH溶液恰好滴定至终点,则测得的盐酸浓度将偏大 | |
| C. | 用镊子夹取金属钠固体,切割取用后剩余的钠放回原试剂瓶中 | |
| D. | 检查容量瓶瓶口是否漏水的方法是:往瓶内加入一定量水,塞好瓶塞.用食指摁住瓶塞,另一只手托住瓶底,把瓶倒转过来,观察瓶塞周围是否有水漏出即可 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 去年12月我国向月球发射的“玉兔号”月亮车,体现了我国航天科技的实力,车上安装的太阳能电池帆板的材料是二氧化硅 | |
| B. | 水泥冶金厂常用高压电除去工厂烟尘,利用了胶体的性质 | |
| C. | 中国食品质量监督局规定,从2011年5月份起,面粉中禁止添加CaO2、过氧化苯甲酰等增白剂,由此说明添加剂均会严重危害人体健康 | |
| D. | 以煤为燃料的工厂、汽车尾气排放物等容易造成雾霾,治理雾霾最好的办法是研制纳米级口罩,以确保肺癌的发病率降低 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 从海水中可提取食盐 | B. | 海水蒸馏可得淡水 | ||
| C. | 直接电解海水可得镁 | D. | 从海水中可提取溴 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com