
【题目】室温下,相同体积的0.5mol·L-1的下列四种溶液:①KCl溶液、②FeCl3溶液、③HF溶液、④Na2CO3溶液,其中所含阳离子数由多到少的顺序是( )
A. ④>①=②>③ B. ①>④>②>③ C. ④>①>③>② D. ④>②>①>③
【答案】D
【解析】
假设溶液体积为1L,分别计算溶液中溶质的物质的量,然后依据强电解质完全电离,弱电解质部分电离,弱碱阳离子、弱酸阴离子部分水解的性质判断解答。
假设溶液体积为1L,浓度均为0.5molL-1相同体积的下列四种溶液,含有KCl 物质的量为0.5mol,氯化钾为强电解质,完全电离所以含有钾离子物质的量为0.5mol;含有FeCl3物质的量为0.5mol,氯化铁为强电解质完全电离产生0.5mol三价铁离子,铁离子为弱碱阳离子,部分水解,所以溶液中三价铁离子水解:Fe3++3OH-![]() Fe(OH)3+3H+,所以阳离子物质的量大于0.5mol;含有HF物质的量为0.5mol,HF为弱电解质,部分电离,所以含有的氢离子小于0.5mol;含有碳酸钠的物质的量为0.5mol,碳酸钠为强电解质完全电离,产生1mol钠离子,所以含有阳离子物质的量为1mol;所以上述溶液中含有阳离子数目由多到少的顺序为:④>②>①>③,故选D。
Fe(OH)3+3H+,所以阳离子物质的量大于0.5mol;含有HF物质的量为0.5mol,HF为弱电解质,部分电离,所以含有的氢离子小于0.5mol;含有碳酸钠的物质的量为0.5mol,碳酸钠为强电解质完全电离,产生1mol钠离子,所以含有阳离子物质的量为1mol;所以上述溶液中含有阳离子数目由多到少的顺序为:④>②>①>③,故选D。


 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案科目:高中化学 来源: 题型:
【题目】福莫特罗是一种治疗哮喘病的药物,它的关键中间体(G)的合成路线如下:

回答下列问题:
(1)F的分子式为_____________,反应①的反应类型为_________。
(2)反应④的化学方程式为___________________________。
(3)C能与FeC13 溶液发生显色反应,C的结构简式为________________, D中的含氧官能团为_________________。
(4)B的同分异构体(不含立体异构)中能同时满足下列条件的共有_____种。
a.能发生银镜反应 b.能与NaOH溶液发生反应 c.含有苯环结构
其中核磁共振氢谱显示为4组峰,且峰面积比为3:2:2:1的是________________(填结构简式)。
(5)参照G的合成路线,设计一种以![]() 为起始原料(无机试剂任选)制备的
为起始原料(无机试剂任选)制备的![]() 合成路线________。
合成路线________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,不属于取代反应的是
A. ![]() +HNO3
+HNO3![]()
![]() +H2O
+H2O
B. CH2=CH2+Br2 ![]() BrCH2CH2Br
BrCH2CH2Br
C. CH4+Cl2![]() CH3Cl+HCl
CH3Cl+HCl
D. CH3CH2CH2Br+NaOH![]() CH3CH2CH2OH+NaBr
CH3CH2CH2OH+NaBr
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,试管中盛装的是红棕色气体(可能是混合物),当倒扣在盛有水的水槽中时,试管内液面上升,但不能充满试管,当向试管内鼓入氧气后,可以观察到试管中液面继续上升,经过多次重复后,试管内完全充满液体,原来试管中盛装的气体是( )
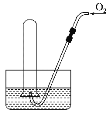
A.可能是N2和NO2的混合气体
B.一定是NO2气体
C.可能是NO与NO2的混合气体
D.只可能是NO2一种气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组利用下面的装置进行实验,②、③中溶液均足量,操作和现象如下表。

实验 | 操作 | 现象 |
Ⅰ | 向盛有Na2S溶液的①中持续通入CO2至过量 | ②中产生黑色沉淀,溶液的pH降低; ③中产生白色浑浊,该浑浊遇酸冒气泡 |
Ⅱ | 向盛有NaHCO3溶液的①中持续通入H2S气体至过量 | 现象同实验Ⅰ |
资料:CaS遇水完全水解
由上述实验得出的结论不正确的是
A. ③中白色浑浊是CaCO3
B. ②中溶液pH降低的原因是:H2S+Cu2+ == CuS↓+2H+
C. 实验Ⅰ①中CO2过量发生的反应是:CO2+H2O+ S2== CO32+ H2S
D. 由实验Ⅰ和Ⅱ不能比较H2CO3和H2S酸性的强弱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
利用丙炔和苯甲醛研究碘代化合物与苯甲醛在 Cr-Ni 催化下可以发生偶联反应和合成 重要的高分子化合物Y的路线如下:

已知:①R1CHO+R2CH2CHO![]()
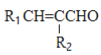 +H2
+H2
②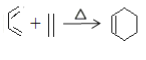
回答下列问题:
(1)A的化学名称为____。
(2)B中含氧官能团的名称是______。
(3)X的分子式为_______。
(4)反应①的反应类型是________。
(5)反应②的化学方程式是_______。
(6)L是D的同分异构体,属于芳香族化合物,与D具有相同官能团,其核磁共振氢谱为5组峰,峰面积比为3:2:2:2:1,则L的结构简式可能为_____。
(7)多环化合物是有机研究的重要方向,请设计由![]() 、CH3CHO、
、CH3CHO、![]() 合成多环化合物
合成多环化合物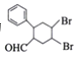 的路线(无机试剂任选)______。
的路线(无机试剂任选)______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图容器底部是培养基,其中含有植物生长所需的全部养分,如果有人在配制培养基的矿质元素中使用了NH4NO3、KNO3、CaCl2·2H2O、MgSO4·7H2O、螯合铁溶液、微量元素溶液,但缺少了一种必需元素,为补充这种元素,应添加的化合物是( )

A.Ca(NO3)2B.KClC.KH2PO4D.K2SO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在给定条件下,下列选项所示的物质间转化均能一步实现的是( )
A. S![]() SO3
SO3![]() H2SO4
H2SO4
B. NH3![]() NO2
NO2![]() HNO3
HNO3
C. Cu2(OH)2CO3![]() CuCl2(aq)
CuCl2(aq)![]() Cu(s)
Cu(s)
D. 饱和NaCl溶液![]() NaHCO3(s)
NaHCO3(s)![]() Na2CO3(s)
Na2CO3(s)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)2SO2(g)+O2(g)![]() 2SO3(g)反应过程的能量变化如图所示。已知1 mol SO2(g)氧化为1 mol SO3(g)的ΔH= 99 kJ/mol。
2SO3(g)反应过程的能量变化如图所示。已知1 mol SO2(g)氧化为1 mol SO3(g)的ΔH= 99 kJ/mol。

请回答下列问题:
①图中A点表示:__________________________。
C点表示:______________________________。
E的大小对该反应的反应热______(填“有”或“无”)影响。
②25℃、101 kPa下测得,2mol SO2和1 mol O2充分反应放出热量________198 kJ(填“大于”、“等于”或“小于”)。
(2)由氢气和氧气反应生成1 mol水蒸气,放出241.8 kJ热量(25℃、101 kPa下测得)
①写出该反应的热化学方程式:_____________________________。
②若1 mol水蒸气转化为液态水放热45kJ,则反应H2(g)+![]() O2(g)
O2(g)![]() H2O( l )的ΔH =________________kJ/mol。
H2O( l )的ΔH =________________kJ/mol。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com