
| A. | 原子序数:a>b>c>d | |
| B. | 离子半径:A(n+1)+>Bn+>C(n+1)->Dn- | |
| C. | 离子氧化性:A(n+1)+>Bn+离子还原性:C(n+1)->Dn- | |
| D. | C最高价氧化物的水化物的酸性比D的强 |
分析 已知aA(n+1)+、bBn+、cC(n+1)-、dDn-均具有相同的电子层结构,则有:a-n-1=b-n=c+n+1=d+n,A、B在周期表中C、D的下一周期,并且原子序数:a>b>d>c,结合元素周期律递变规律解答该题.
解答 解:A.aA(n+1)+、bBn+、cC(n+1)-、dDn-均具有相同的电子层结构,则有:a-n-1=b-n=c+n+1=d+n,则有A、B在周期表中C、D的下一周期,并且原子序数:a>b>d>c,故A错误;
B.具有相同电子层结构的离子,原子序数大的离子半径小,则离子半径大小为:C(n+1)->Dn->Bn+>A(n+1)+,故B错误;
C.金属性越强,对应离子的氧化性越弱,非金属性越强,对应离子的还原性越强,则离子还原性为:C(n+1)->Dn-,离子氧化性为Bn+<A(n+1)+,故C正确;
D.非金属性D>C,D最高价氧化物的水化物的酸性比C的强,故D错误.
故选C.
点评 本题考查原子结构与元素周期律的关系,题目难度中等,明确核外电子排布确定元素所在周期表中的位置以及把握元素周期律的递变规律是解答该题的关键,试题培养了学生的灵活应用能力.


 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 95℃纯水的pH<7,说明加热可导致水呈酸性 | |
| B. | pH=3的醋酸溶液稀释至10倍后pH=4 | |
| C. | 0.2 mol/L的盐酸与0.1 mol/L的盐酸等体积混合后pH=1.5 | |
| D. | 若向氨水中加入等浓度稀盐酸至溶液正好呈中性,则所用稀盐酸的体积一定小于氨水的体积 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 放电过程中,负极每消耗1mol Al,导线中转移的电子数为3NA(NA为阿伏伽德罗常数的值) | |
| B. | 放电时,负极反应式为Al+7[AlCl4]--3e-=4[Al2Cl7]- | |
| C. | 充电时,阴极反应式为Cn[AlCl4]+e-=[AlCl4]-+Cn | |
| D. | 充、放电过程中,R+的移动方向相反 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④⑤ | B. | ①③⑤ | C. | ①②③⑤ | D. | ①③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②⑤ | B. | ②③⑤ | C. | ③④⑤ | D. | ②④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 以上反应均可发生 | B. | 只有⑦不能发生 | ||
| C. | 只有⑤不能发生 | D. | 只有⑥不能发生 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题


 ,反应类型:消去反应;
,反应类型:消去反应;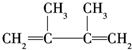 +Br2→CH2BrCBr(CH3)(CH3)C=CH2,反应类型:加成反应.
+Br2→CH2BrCBr(CH3)(CH3)C=CH2,反应类型:加成反应.查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | ①说明水解反应为放热反应 | B. | ③说明水解反应为吸热反应 | ||
| C. | ①中溶液红色变浅 | D. | ③中溶液红色变深 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com