
| A. | C(s)+$\frac{1}{2}$O2(g)═CO(g)△H=+110.5 kJ•mol-1 | |
| B. | C(s)+O2(g)═CO2(g)△H=-393.5 kJ•mol-1 | |
| C. | 2H2(g)+O2(g)═2H2O(l)△H=-571.6 kJ•mol-1 | |
| D. | H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H=-241.8 kJ•mol-1 |
分析 燃烧热是指1mol纯净物完全燃烧生成稳定的氧化物放出的热量,
A.碳的燃烧为放热反应,焓变应该小于0;
B.根据燃烧热的概念及热化学方程式的书写原则分析;
C.氢气燃烧热的热化学方程式中,氢气的计量数必须为1;
D.氢气的燃烧热中,生成水的状态必须液态.
解答 解:A.C燃烧生成的稳定氧化物是CO2不是CO,且焓变为负值,所以不符合燃烧热的概念要求,故A错误;
B.1molC完全燃烧生成稳定的CO2,符合燃烧热的概念要求,该反应放出的热量为燃烧热,故B正确;
C.燃烧热是指1mol纯净物完全燃烧,方程式中氢气的系数为2mol,不是氢气的燃烧热,故C错误;
D.燃烧热的热化学方程式中生成的氧化物必须为稳定氧化物,水为液态时较稳定,故D错误;
故选B.
点评 本题考查热化学方程式的书写方法,题目难度不大,明确燃烧热达到概念为解答关键,注意掌握热化学方程式的书写原则,试题培养了学生的灵活应用能力.


 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 明矾净水 | |
| B. | 由豆浆制豆腐 | |
| C. | 一束平行光照射蛋白质溶液时,从侧面看到光亮的“通路” | |
| D. | 向FeCl3溶液中滴入NaOH溶液,出现红褐色沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1 mol/L NaB溶液中水电离的OH-浓度大于10-7 mol/L | |
| B. | NaB溶液中:c(Na+)>c(B-)>c(H+)>c(OH-) | |
| C. | NaB溶液中:c(Na+)+c(H+)=c(HB)+c(B-) | |
| D. | HB的电离方程式为:HB═H++B- |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钠、镁等金属着火,不可用CO2灭火 | |
| B. | 在气体发生装置上点燃氢气等气体时,必须先检验气体的纯度 | |
| C. | 实验结束后将所有的废液倒入下水道排出实验室,以免污染实验室 | |
| D. | 给试管中的液体加热时,不停沿试管倾斜方向移动试管或加入碎瓷片,以免液体暴沸伤人 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 32g氧气和臭氧混合物中氧原子的物质的量为2 mol | |
| B. | 2mol的硫酸的摩尔质量为196g/mol | |
| C. | 一定温度和压强下,各种气态物质的体积由构成气体分子的大小决定 | |
| D. | 将58.5gNaCl溶于941.5g水中配成1mol/L的NaCl溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
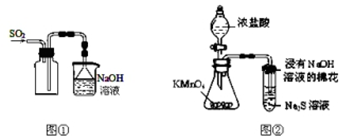
| A. | 实验室采用图①所示装置收集SO2 | |
| B. | 除去NaHCO3溶液中的Na2CO3,可加入Ca(OH)2溶液后过滤 | |
| C. | 称取0.40 g NaOH,置于100 mL容量瓶中,加水溶解,配制0.10 mol/L NaOH溶液 | |
| D. | 可用图②所示装置比较KMnO4、Cl2、S的氧化性强弱 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com