
| A. | 0.1mol | B. | 0.01mol | C. | 6.5g | D. | 5.6g |
分析 在托盘天平的两个托盘上放两个质量相同的烧杯,并在烧杯中分别加入100mL 1mol•L-1硫酸即0.1mol.现在在天平右盘的烧杯里放入0.1mol锌,则锌和硫酸能恰好完全反应生成0.1mol氢气,故右盘增重的质量为6.5g-0.2g=6.3g.若在左盘加入铁,由于铁的摩尔质量小于锌,为56g/mol,故若想增重6.3g,则加入的铁的物质的量应大于0.1mol,据此分析计算.
解答 解:在托盘天平的两个托盘上放两个质量相同的烧杯,并在烧杯中分别加入100mL 1mol•L-1硫酸即0.1mol.现在在天平右盘的烧杯里放入0.1mol锌,则锌和硫酸能恰好完全反应生成0.1mol氢气,故右盘增重的质量为6.5g-0.2g=6.3g.为了保持天平平衡,则左盘也应增重6.3g.若在左盘加入铁,由于铁的摩尔质量小于锌,为56g/mol,故若想增重6.3g,则加入的铁的物质的量应大于0.1mol.
设左盘加入铁的物质的量为xmol,则一定有x>0.1mol,故铁0.1mol硫酸反应时,铁过量,生成氢气的量由硫酸决定,故为0.1mol,故左盘增重的质量为:
56g/mol×xmol-0.1mol×2g/mol=6.3g
解得x=$\frac{6.5g}{56g/mol}$=$\frac{6.5}{56}$mol
质量m=$\frac{6.5}{56}mol×56g/mol$=6.5g,故选C.
点评 本题考查了金属和酸反应后溶液的增重问题,应首先判断出铁的物质的量需大于锌的物质的量,然后根据当一种物质过量时,应根据量少的物质来计算产物的量来分析.


 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案 应用题作业本系列答案
应用题作业本系列答案科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
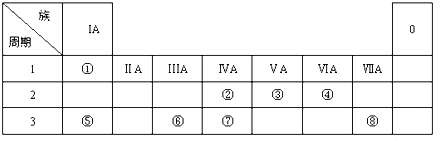
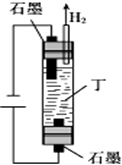 6种相邻短周期主族元素的相对位置如下表,M元素原子核外电子数是Y元素原子核外电子数的2倍,W元素原子的次外层电子数是最外层电子数的2倍.用化学用语回答下列问题:
6种相邻短周期主族元素的相对位置如下表,M元素原子核外电子数是Y元素原子核外电子数的2倍,W元素原子的次外层电子数是最外层电子数的2倍.用化学用语回答下列问题:| X | Y | Z | |
| W | M | Q |
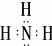 ,实验室制备甲的化学方程式是2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O,甲可以与X的最高价氧化物对应的水化物溶液反应生成盐乙,乙溶液中的离子浓度由大到小的顺序是c(NO3-)>c(NH4+)>c(H+)>c(OH-).X的含18个电子的气态氢化物丙可与空气构成一种环保型碱性燃料电池,电池工作时丙发生的电极反应方程式是N2H4-4e-+4OH-═N2+4H2O.
,实验室制备甲的化学方程式是2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O,甲可以与X的最高价氧化物对应的水化物溶液反应生成盐乙,乙溶液中的离子浓度由大到小的顺序是c(NO3-)>c(NH4+)>c(H+)>c(OH-).X的含18个电子的气态氢化物丙可与空气构成一种环保型碱性燃料电池,电池工作时丙发生的电极反应方程式是N2H4-4e-+4OH-═N2+4H2O.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径:Cl>P | B. | 氢化物的稳定性:CH4<SiH4 | ||
| C. | 金属性强弱:Na>Li | D. | 酸性:H2CO3>H3PO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| X | Y | |
| Z | W |
| A. | 元素W位于第三周期第ⅤA族 | |
| B. | 元素Y的氢化物水溶液呈酸性 | |
| C. | 元素X、Z的各种氯化物分子中,各原子均满足8电子稳定结构 | |
| D. | 元素X与氢元素形成的原子个数比为1:1的化合物有多种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2O(g)═H2(g)+$\frac{1}{2}$O2(g)△H=-485 kJ•mol-1 | B. | H2O(g)═H2(g)+$\frac{1}{2}$O2(g)△H=485 kJ•mol-1 | ||
| C. | 2H2(g)+O2(g)═2H2O(g)△H=485 kJ•mol-1 | D. | 2H2(g)+O2(g)═2H2O(g)△H=-485 kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
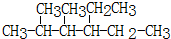 2,3-二甲基-3-乙基己烷
2,3-二甲基-3-乙基己烷 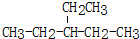 2-乙基戊烷
2-乙基戊烷查看答案和解析>>
科目:高中化学 来源: 题型:实验题
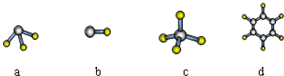
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 药品橱 | 甲 | 乙 | 丙 | 丁 |
| 药品 | 锌、铜 | 硫酸钠 | 氢氧化钠 | 盐酸 |
| 铁、镁 | 碳酸钠 | 氢氧化钾 | 稀硫酸 |
| A. | 甲橱 | B. | 乙橱 | C. | 丙橱 | D. | 丁橱 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com