
【题目】容量瓶是用来配制物质的量浓度溶液的定量仪器,其上标有:①温度 ②浓度 ③容量 ④压强 ⑤刻度线,这五项中的( )
A. ②④⑤B. ②③⑤C. ①③⑤D. ①②⑤
科目:高中化学 来源: 题型:
【题目】元素铬(Cr)在溶液中主要以Cr3+(蓝紫色)、Cr(OH)![]() (绿色)、Cr2O72-(橙红色)、CrO42-(黄色)等形式存在。Cr(OH)3为难溶于水的灰蓝色固体。回答下列问题:
(绿色)、Cr2O72-(橙红色)、CrO42-(黄色)等形式存在。Cr(OH)3为难溶于水的灰蓝色固体。回答下列问题:
(1)Cr3+与Al3+的化学性质相似。在Cr2(SO4)3溶液中逐滴加入NaOH溶液直至过量,可观察到的现象是________________________;
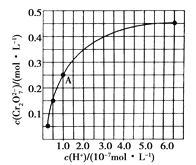
(2)CrO42-和Cr2O72-在溶液中可相互转化。室温下初始浓度为1.0 mol·L-1的Na2CrO4溶液中c(Cr2O72-)随c(H+)的变化如上图所示。
①用离子方程式表示Na2CrO4溶液中的转化反应_____________________;
②由图可知,溶液酸性增大,CrO42-的平衡转化率________(填“增大”“减小”或“不变”)。根据A点数据,计算出该转化反应的平衡常数为___________;
③升高温度,溶液中CrO42-的平衡转化率减小,则该反应的ΔH________0(填“大于”“小于”或“等于”)。
(3)在化学分析中采用K2CrO4为指示剂,以AgNO3标准溶液滴定溶液中Cl-,利用Ag+与CrO42-生成砖红色沉淀,指示滴定终点的到达。当溶液中Cl-恰好沉淀完全(Cl-浓度等于1.0×10-5mol·L-1)时,溶液中c(Ag+)为________mol·L-1,此时溶液中c(CrO![]() )等于________mol·L-1。(已知Ag2CrO4、AgCl的Ksp分别为2.0×10-12和2.0×10-10)。
)等于________mol·L-1。(已知Ag2CrO4、AgCl的Ksp分别为2.0×10-12和2.0×10-10)。
(4)+6价铬的化合物毒性较大,常用NaHSO3将废液中的Cr2O72-还原成Cr3+,该反应的离子方程式为_______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于芳香烃的叙述中正确的是( )
A.其组成的通式是CnH2n-6(n≥6)
B.分子里含有苯环的烃
C.分子里含有苯环的各种有机物
D.苯及其同系物的总称
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】YBa2Cu8Ox(Y为钇元素)是磁悬浮列车中的重要超导材料,关于 ![]() Y的说法正确的是( )
Y的说法正确的是( )
A.钇在周期表中的位置是第4周期ⅢB族
B.属于非金属元素
C.![]() Y和
Y和 ![]() Y是两种不同的核素
Y是两种不同的核素
D.中子数为39
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨是最重要的氮肥,是产量最大的化工产品之一,其合成原理为:N2(g)+3H2(g)![]() 2NH3(g) ΔH=-92.4 kJ·mol-1。在密闭容器中,使2 mol N2和6 mol H2混合发生下列反应:
2NH3(g) ΔH=-92.4 kJ·mol-1。在密闭容器中,使2 mol N2和6 mol H2混合发生下列反应:
N2(g)+3H2(g)![]() 2NH3(g)(正反应为放热反应)
2NH3(g)(正反应为放热反应)
(1)当反应达到平衡时,N2和H2的浓度比是______;N2和H2的转化率比是______。
(2)升高平衡体系的温度(保持体积不变),混合气体的平均相对分子质量______,密度______。(填“变大”“变小”或“不变”)
(3)当达到平衡时,充入氩气,并保持压强不变,平衡将______ (填“正向”“逆向”或“不”)移动。
(4)若容器恒容、绝热,加热使容器内温度迅速升至原来的2倍,平衡将______ (填“向左移动”“向右移动”或“不移动”)。达到新平衡后,容器内温度______ (填“大于”“小于”或“等于”)原来的2倍。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在酸性溶液中,下列离子能大量共存的是
A. NH4+、Ba2+、SO42-、Cl-B. K+、Fe3+、Cl-、OH-
C. K+、Na+、CO32-、SO42-D. Na+、K+、NO3-、SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、M、Z、R为前四周期元素,且原子序数依次增大。XY2是红棕色气体;X与氢元素可形成XH3;M是周期表中电负性最大的元素;Z基态原子的M层是K层电子数的3倍;R2+的3d轨道中有9个电子。请回答下列问题:
(1)基态Y原子核外有___________种不同运动状态的电子;
Z所在周期中第一电离能最大的主族元素是____(写元素名称)。
(2)离子X Y-的立体构型是_____;,X2M2分子中X原子的杂化方式是______,1 molX2M2含有___________个σ键;
(3)向RZO4的水溶液中逐滴加入氨水至过量,观察到溶液由天蓝色最终变为_____色。反应过程中涉及的离子方程式为:______________________、__________________________。
(4) 从核外电子排布角度解释高温下R2O比RO更稳定的原因 _____________________________
(5)已知XH3易与R2+形成配离子,但XM3不易与R2+形成配离子,其原因是_______________________________________________。
(6)如图表示某种含氮有机化合物的结构,其分子内4个氮原子分别位于正四面体的4个顶点(见如图),分子内存在空腔,能嵌入某离子或分子并形成4个氢键予以识别。下列分子或离子中,能被该有机化合物识别的是____(填字母)。
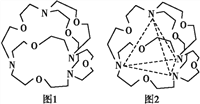
a.CF4 b.CH4 c.NH4+ d.H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某混合溶液中,可能大量含有的离子如下表:
阳离子 | H+、K+、Al3+、NH4+、Mg2+ |
阴离子 | OH-、SO42-、CO32-、AlO2- |
将Na2O2逐渐加入上述混合溶液中并微热(忽略溶液体积变化及水蒸气的影响),产生沉淀和气体如图所示。
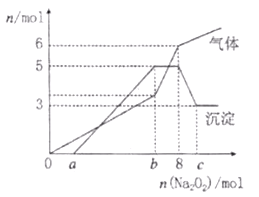
请根据信息回答下列问题:
(1)将上述混合溶液中一定大量含有的阴、阳离子及其物质的量填入下表(可以不填满,也可以增加):____
离子种类 | ||||||
物质的量(mol) |
(2)图中a=____;b=____;c=____.
(3)简述溶液中还可能大量含有的离子的鉴定方法:____.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com