
V L Fe2(SO4)3溶液中含Fe3+ m g,则溶液中SO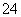 的物质的量浓度为 ( )
的物质的量浓度为 ( )
A.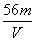 mol·L-1 B.
mol·L-1 B.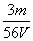 mol·L-1
mol·L-1
C.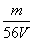 mol·L-1 D.
mol·L-1 D.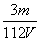 mol·L-1
mol·L-1
科目:高中化学 来源: 题型:
判断下列有关化学基本概念的依据正确的是( )
A.置换反应:是否有单质参加
B.纯净物与混合物:是否仅含有一种元素
C.溶液与胶体:本质区别是分散质粒子的直径大小
D.电解质与非电解质:物质本身是否具有导电性
查看答案和解析>>
科目:高中化学 来源: 题型:
短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图所示。下列说法正确的是( )

A.元素X与元素Z的最高正化合价之和的数值等于8
B.原子半径的大小顺序为:rX>rY>rZ>rW>rQ
C.离子Y2-和Z3+的核外电子数和电子层数都不相同
D.元素W的最高价氧化物对应的水化物的酸性比Q的强
查看答案和解析>>
科目:高中化学 来源: 题型:
一种新型燃料电池,一极通入空气,另一极通入丁烷气体;电解质是掺杂氧化钇(Y2O3)的氧化锆(ZrO2)晶体,在熔融状态下能传导O2-。下列对该燃料电池说法正确的是( )
A.在熔融电解质中,O2-由负极移向正极
B.通入丁烷的一极是正极,电极反应为:2C4H10+26e-+13O2-=4CO2+5H2O
C.通入空气的一极是负极,电极反应为:O2+4e-=2O2-
D.电池的总反应是:2C4H10+13O2 = 8CO2+10H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
某化学反应2A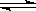 B+D在四种不同条件下进行,B、D起始浓度为0。反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表:
B+D在四种不同条件下进行,B、D起始浓度为0。反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表:
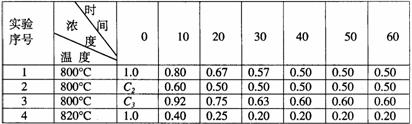 |
根据上述数据,完成下列填空:
(1)在实验1,反应在10至20分钟时间内平均速率为 mol/(L·min)。
(2)在实验2,A的初始浓度c2= mol/L,反应经20分钟就达到平衡,可推测实验2中还隐含的条件是 。
(3)设实验3的反应速率为v3,实验1的反应速率为v1,则v3 v1
(填>、=、<)。
(4)实验2达到平衡时,A的平衡转化率为
查看答案和解析>>
科目:高中化学 来源: 题型:
用6.02×1023表示阿伏加德罗常数的值,下列说法中正确的是 ( )
A.常温常压下,1.6 g臭氧中含有6.02×1022个氧原子
B.标准状况下,2.24 L水中含有6.02×1022个水分子
C.2.24 L氨气分子中含6.02×1023个电子
D.18g D2O中所含的中子数为10NA
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)下列物质:①NaCl晶体 ②SO3 ③冰醋酸 ④铜 ⑤BaSO4固体
⑥纯蔗糖⑦酒精 ⑧熔融的KNO3 ⑨空气,⑩食盐水,
请回答下列问题(用序号填空):
(Ⅰ)能导电的是____________________________;
(Ⅱ)属于电解质的是____________________________;
(Ⅲ)属于非电解质的是____________________________;
(Ⅳ)溶于水后形成的溶液能导电的是____________________________。
(2)18g NH4+中含有氢原子的物质的量是_____________;含有质子的物质的量是_____________;含有电子的数目是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
依据元素周期表及元素周期律,下列推断正确的是( )
A.H3BO3的酸性比H2CO3的强
B.Mg(OH)2的碱性比Be(OH)2的强
C.HCl、HBr、HI的热稳定性依次增强
D.若M+和R2-的核外电子层结构相同,则原子序数:R>M
查看答案和解析>>
科目:高中化学 来源: 题型:
图中每一方格表示有关的一种反应物或生成物。已知B是一种单质,其余物质都是含有B元素的化合物;C是一种钠盐;E是C对应的酸;B和D的晶体都是高熔点、坚硬的固体,且D为B的氧化物(其他不含B元素的反应物以及各步反应添加的必要试剂和反应条件均被略去)。

(1)写出A、D、E的化学式:
A________________________________________________________________________;
D________________________________________________________________________;E__________________。
(2)在工业上,用碳在高温下还原D的方法可制得含少量杂质的B,其化学反应方程式为
________________________________________________________________________;
A和B的互变在工业上的实际意义是
________________________________________________________________________
________________________。
(3)写出D―→C反应的离子方程式_________________________________________
________________________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com