


 全能测控一本好卷系列答案
全能测控一本好卷系列答案科目:高中化学 来源: 题型:
| A、蔬菜 | B、谷类 | C、奶类 | D、肉类 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
 ,这是21世纪具有广阔前景的合成材料.
,这是21世纪具有广阔前景的合成材料.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
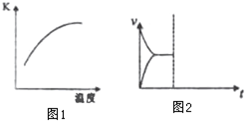 科学家一直致力于“人工固氮”的新方法研究.
科学家一直致力于“人工固氮”的新方法研究.| v(N2) |
| v(O2) |
| c(OH-) |
| c(NH3?H2O) |
| c(H+) |
| c(OH-) |
| m |
| n |
| m |
| n |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ① | H2(g)+O2(g)═H2O(g)△H═-242kJ/mol; |
| ② | 2H2(g)+O2(g)═2H2O(l)△H═-572kJ/mol; |
| ③ | C(s)+O2(g)═CO(g)△H═-110.5kJ/moL; |
| ④ | C(s)+O2(g)═CO2(g)△H═-393.5kJ/moL; |
| ⑤ | CO2(g)+2H2O(g)═CH4(g)+2O2(g)△H═+802kJ/moL |
| 化学键 | O=O | C-C | H-H | O-O | C-O | O-H | C-H |
| 键能kJ/mol | 497 | 348 | 436 | 142 | 351 | 463 | 414 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com