
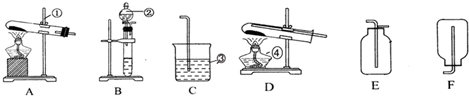
分析 (1)根据仪器的图形、构造判断仪器的名称;
(2)实验室可用加热高锰酸钾固体制备氧气,用稀硫酸和锌反应制备氢气,氢气密度比空气小,可用向下排空法收集氢气;
(3)做木炭还原氧化铜并检验生成气体的实验,可在大试管中加热条件下进行,用澄清石灰水检验;
(4)用稀硫酸和锌反应制备氢气,在大试管中加热条件下进行还原实验,实验结束时应先停止加热,待试管冷却后,再停止通氢气,防止铜被氧化
解答 解:(1)由仪器的图形、构造判断①~④的仪器名称分别为铁架台、分液漏斗、烧杯、酒精灯,故答案为:铁架台;分液漏斗;烧杯;酒精灯;
(2)实验室可用加热高锰酸钾固体制备氧气,氧气密度比空气大,可用向上排空法收集,则选用A、E装置,用稀硫酸和锌反应制备氢气,氢气密度比空气小,可用向下排空法收集氢气,则选用B、F装置,故答案为:A;E;B;F;
(3)做木炭还原氧化铜并检验生成气体的实验,可在大试管中加热条件下进行,用澄清石灰水检验,可用D、C装置,可观察到澄清石灰水变浑浊,故答案为:澄清的石灰水;C中澄清石灰水变浑浊;
(4)用稀硫酸和锌反应制备氢气,在大试管中加热条件下进行还原实验,可用B、D装置,实验结束时应先停止加热,待试管冷却后,再停止通氢气,防止铜被氧化.
故答案为:B;D;防止铜被氧化.
点评 本题主要考查物质的制备以及性质检验,为高频考点,侧重于学生的分析、实验能力的考查,要想解答好这类题目,就要熟记常用气体的发生装置和收集装置与选取方法及其依据,还有氧气、二氧化碳的实验室制取方法,有时还需弄清图示信息等等.


科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
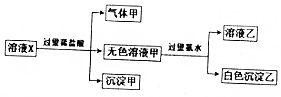 水溶液中只可能有K+、Mg2+、AlO2-、Al3+、SiO32-、CO32-、SO42-中的若干种离子,某同学对溶液进行了如下实验:下列判断错误的是( )
水溶液中只可能有K+、Mg2+、AlO2-、Al3+、SiO32-、CO32-、SO42-中的若干种离子,某同学对溶液进行了如下实验:下列判断错误的是( )| A. | 溶液X可能含有Mg2+或Al3+ | |
| B. | 沉淀甲只可能是硅酸沉淀 | |
| C. | 有气体甲生成,表明溶液X中一定含有CO32- | |
| D. | 不能确定SO42-是否存在于溶液X中 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子核外电子数为3 | B. | 相对原子质量为2 | ||
| C. | 原子的核电荷数为3 | D. | 原子结构示意图为  |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用过滤的方法除去食盐水中的泥沙 | |
| B. | 用分液的方法分离乙醇和水的混合物 | |
| C. | 用萃取的方法提取碘水中的碘 | |
| D. | 用结晶的方法分离氯化钠和硝酸钾的混合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com