
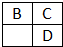
 A、B、C、D、E均为短周期主族元素,B、C、D在周期表中的位置关系如图所示.A是短周期中原子半径最小的元素,A、B、C三种元素的原子序数之和等于D元素的原子序数,E是短周期中最活泼的金属元素.下列说法错误的是( )
A、B、C、D、E均为短周期主族元素,B、C、D在周期表中的位置关系如图所示.A是短周期中原子半径最小的元素,A、B、C三种元素的原子序数之和等于D元素的原子序数,E是短周期中最活泼的金属元素.下列说法错误的是( )| A、简单离子的半径大小关系:B>C>E |
| B、D元素的气态氢化物比C元素的气态氢化物稳定 |
| C、由A、B、C三种元素组成的离子化合物NH4NO3中,阴、阳离子个数比为1:1 |
| D、由C、D、E三种元素组成的某种化合物,水解显碱性 |


科目:高中化学 来源: 题型:
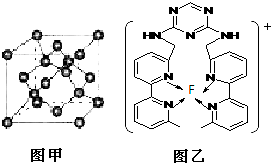 现有A、B、C、D、E、F原子序数依次增大的六种元素,它们位于元素周期表的前四周期.A元素能级个数与核外电子数相等,B元素含有3个能级,且每个能级所含的电子数相同;D的原子核外有8个运动状态不同的电子;E元素与F元素处于同一周期相邻的族,它们的原子序数相差3,且E元素的基态原子有4个未成对电子.请回答下列问题:
现有A、B、C、D、E、F原子序数依次增大的六种元素,它们位于元素周期表的前四周期.A元素能级个数与核外电子数相等,B元素含有3个能级,且每个能级所含的电子数相同;D的原子核外有8个运动状态不同的电子;E元素与F元素处于同一周期相邻的族,它们的原子序数相差3,且E元素的基态原子有4个未成对电子.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、③④ | B、①③④ |
| C、②③④ | D、①②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、化学反应中的能量变化通常表现为热量的变化 |
| B、化学键的断裂和形成是化学反应中能量变化的主要原因 |
| C、反应物总能量和生成物总能量的相对大小决定了反应是放出能量还是吸收能量 |
| D、需要加热才能发生的化学反应一定是吸热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、 |
B、 |
C、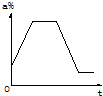 |
D、 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、除去工业废水中的Cu2+可以选用FeS作沉淀剂 |
| B、将足量CuSO4溶解在0.1mol?L-1 H2S溶液中,Cu2+的最大浓度为1.3×10-35mol?L-1 |
| C、因为H2SO4是强酸,所以反应CuSO4+H2S═CuS↓+H2SO4不能发生 |
| D、向H2S的饱和溶液中通入少量SO2气体溶液的酸性增强 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Mg2+、Na+、CO32-、I- |
| B、Al3+、Na+、SO32-、I- |
| C、Al3+、Mg2+、SO32-、I- |
| D、Al3+、CO32-、Br-、SO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、由1mol CH3COONa和少量CH3COOH形成的中性溶液中,CH3COO-数目为NA个 |
| B、常温常压下,14g由N2与CO组成的混合气体含有的原子数目为NA |
| C、标准状况下,6.72L NO2与水充分反应转移的电子数目为0.2NA |
| D、2mol SO2和1mol O2在一定条件下充分反应后,所得混合气体的分子数小于2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、甲、丁、戊的单质都是金属 |
| B、乙、丙、辛都是非金属元素 |
| C、乙、庚、辛都能形成氧化物 |
| D、己的氧化物既可溶于KOH溶液又可溶于H2SO4溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com