
分析 (1)向沸水中滴入几滴饱和FeCl3溶液,继续煮沸至溶液呈红褐色,即制得Fe(OH)3胶体;
(2)胶体和溶液是不同的分散系,胶体有丁达尔效应溶液没有;
(3)向Fe(OH)3胶体中滴入稀盐酸,先发生胶体的聚沉,然后二者之间会发生复分解反应.
解答 解:(1)实验室制备氢氧化铁胶体是在沸腾的蒸馏水中加入饱和氯化铁溶液,当溶液变为红褐色时立即停止加热,反应的化学方程式为FeCl3+3H2O$\frac{\underline{\;\;△\;\;}}{\;}$Fe(OH)3(胶体)+3HCl,
故答案为:红褐;FeCl3+3H2O$\frac{\underline{\;\;△\;\;}}{\;}$Fe(OH)3(胶体)+3HCl;
(2)胶体具有丁达尔效应,故而溶液没有,故可以看到乙烧杯中的液体产生丁达尔效应;这个实验可以用来区别胶体和溶液;
故答案为:乙;胶体和溶液;
(3)①向Fe(OH)3胶体中滴入稀盐酸,先发生胶体的聚沉,产生红褐色沉淀,故答案为:聚沉;
②向Fe(OH)3胶体中滴入稀盐酸,先发生胶体的聚沉,产生红褐色沉淀,继续滴入然后二者之间会发生复分解反应,得到棕黄色溶液,反应的离子方程式:Fe(OH)3+3H+=Fe3++3H2O,
故答案为:Fe(OH)3+3H+=Fe3++3H2O.
点评 本题考查氢氧化铁胶体的制备和性质,以及相关化学方程式和离子方程式的书写,难度中等.了解胶体的制备及性质是解题关键.


科目:高中化学 来源: 题型:多选题
| A. | 白磷转化为红磷是吸热反应 | B. | 白磷比红磷稳定 | ||
| C. | 红磷转化为白磷为吸热反应 | D. | 红磷比白磷稳定 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
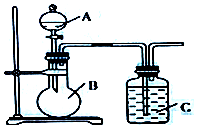
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
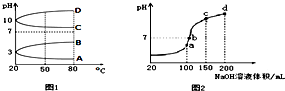 NH4Al(SO4)2是食品加工中最为快捷的食品添加剂,用于焙烤食品中;NH4HSO4在分析试剂、医药、电子工业中用途广泛.请回答下列问题:
NH4Al(SO4)2是食品加工中最为快捷的食品添加剂,用于焙烤食品中;NH4HSO4在分析试剂、医药、电子工业中用途广泛.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 含有较多Fe3+的溶液:Na+、SO42-、HS-、NH4+ | |
| B. | pH=1的溶液:K+、Fe2+、NO3-、Na+ | |
| C. | c(OH-)=1mol•L-1的溶液:AlO2-、CH3COO-、K+、Ba2+ | |
| D. | 遇Al能放出H2的溶液:HCO3-、K+、Mg2+、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0 | B. | +3 | C. | +4 | D. | +5 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com