
)向硝酸钠溶液中加入铜粉不发生反应,若再加入(或通入)某种物质,则铜粉可以逐渐溶解,不符合此条件的物质是( )
|
| A. | Fe(NO3)3 | B. | HCl | C. | NaHSO4 | D. | NaHCO3 |
考点:
铜金属及其重要化合物的主要性质.
专题:
几种重要的金属及其化合物.
分析:
A、依据铜可以与Fe3+发生氧化还原反应分析;
B、依据加入盐酸,即加入H+,H+与硝酸钠中的NO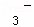 构成硝酸,能氧化铜分析;
构成硝酸,能氧化铜分析;
C、依据硫酸氢钠电离出H+,与B原理相同分析;
D、依据碳酸氢钠为弱酸的盐,不能电离出H+分析.
解答:
解:A、铜可以与Fe3+发生氧化还原反应生成亚铁离子和铜离子,故符合,故A不选择;
B、硝酸钠中加入盐酸,即加入H+,H+与NO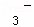 构成硝酸,能氧化铜,使铜溶解,故符合,B不选择;
构成硝酸,能氧化铜,使铜溶解,故符合,B不选择;
C、NaHSO4=Na++H++SO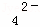 ,H+与硝酸钠中的NO
,H+与硝酸钠中的NO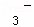 构成硝酸,能氧化铜,使铜溶解,故符合,C不选择;
构成硝酸,能氧化铜,使铜溶解,故符合,C不选择;
D、碳酸氢钠为弱酸盐,不能电离出氢离子,故不符合条件,D选择;故答案为D.
点评:
本题主要考查的是铜的化学性质,属于常考题,需要同学们平时多总结.


 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案科目:高中化学 来源: 题型:
莽草酸可用于合成药物达菲,其结构简式如图,下列关于莽草酸的说法正确的是()
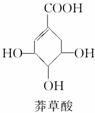
A. 分子式为C7H6O5
B. 1mol莽草酸最多能和4molNaOH中和
C. 分子中含有3种官能团
D. 在水溶液中羧基和羟基均能电离出H+
查看答案和解析>>
科目:高中化学 来源: 题型:
对于反应N2+O2⇌2NO在密闭容器中进行,下列哪个条件不能加快化学反应速率( )
|
| A. | 缩小体积使压强增大 |
|
| B. | 体积不变充入N2使压强增大 |
|
| C. | 体积不变充入 He使压强增大 |
|
| D. | 升高温度 |
查看答案和解析>>
科目:高中化学 来源: 题型:
Na2S的水溶液洗患处可以用来治疗由一种小芥虫在皮肤内生活引起的皮肤病,而且用热水配制的Na2S溶液治疗效果更好.请说明原因,并写出有关的离子方程式.(已知:H2S有毒,可杀虫)
(1)可治疗的原因
(2)热水配制的原因 .
(3)离子方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
如图为某化学反应的速率与时间的关系示意图.在t1时刻升高温度或增大压强,速率的变化都符合示意图的反应是( )
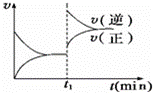
|
| A. | 2SO2(g)+O2(g)⇌2SO3(g);△H<0 |
|
| B. | 4NH3(g)+5O2(g)⇌4NO(g)+6H2O(g);△H<0 |
|
| C. | H2(g)+I2(g)⇌2HI(g);△H>0 |
|
| D. | C(s)+H2O(g)⇌CO(g)+H2(g);△H>0 |
查看答案和解析>>
科目:高中化学 来源: 题型:
如图为装有活塞(质量忽略不计)的密闭容器,内盛22.4mL一氧化氮,若通入11.2mL氧气(气体体积均在标准状况下测定),保持温度压强不变,则容器内的密度为(提示:不考虑NO转化为NO2的可逆性)( )
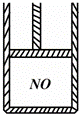
|
| A. | 等于1.369g•L﹣1 |
|
| B. | 等于2.054g•L﹣1 |
|
| C. | 在1.369g•L﹣1和2.054g•L﹣1之间 |
|
| D. | 在2.054g•L﹣1和4.108g•L﹣1之间 |
查看答案和解析>>
科目:高中化学 来源: 题型:
已知分解1mol H2O2放出热量98kJ,在含少量I﹣的溶液中,H2O2分解的机理为:
H2O2+I﹣→H2O+IO﹣ 慢
H2O2+IO﹣→H2O+O2+I﹣ 快
下列有关该反应的说法正确的是()
A. 反应速率与I﹣的浓度有关 B. IO﹣也是该反应的催化剂
C. 反应活化能等于98kJ•mol﹣1 D. v(H2O2)=v(H2O)=v(O2)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com