
| A. | 对于一定条件下已平衡的可逆反应,增加反应物的物质的量,正反应速率一定增大 | |
| B. | 改变外界条件使化学反应速率发生改变,则化学平衡一定发生移动 | |
| C. | 催化剂能改变活化分子百分数,所以一定可以改变化学反应速率和化学平衡 | |
| D. | 升高温度,正、逆反应速率均增大,平衡向吸热反应方向移动 |
科目:高中化学 来源: 题型:解答题
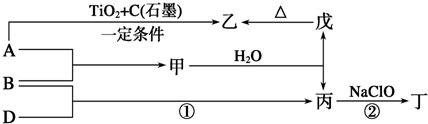
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③⑥ | B. | ②③④⑥ | C. | ①④⑤⑥ | D. | ②⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 人们可以利用先进的化学技术和设备制造新的原子 | |
| B. | 人们可以利用催化剂使水变成汽油 | |
| C. | 人们可以利用先进的化学技术和设备制造自然界中不存在的分子 | |
| D. | 化学科学只能通过实验来探究物质的性质 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 物质 | Fe(OH)2 | Cu(OH)2 | Fe(OH)3 |
| Ksp/25℃ | 8.0×10-16 | 2.2×10-29 | 4.0×10-38 |
| 完全沉淀时的pH范围 | ≥9.6 | ≥6.4 | 3~4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  | B. | 对二甲苯 | C. |  | D. |  |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 某盐溶液中加入NaOH溶液有白色沉淀出现,则原溶液中一定含有Mg2+ | |
| B. | 某溶液中加入AgNO3溶液有白色沉淀出现,则原溶液中一定含有Cl- | |
| C. | 某溶液中加入盐酸产生能使澄清石灰水变浑浊的无色无味的气体,则原溶液中一定含有${CO}_{3}^{2-}$和${HCO}_{3}^{-}$中的一种 | |
| D. | 某盐溶液中加入NaOH溶液并加热,能产生使湿润的蓝色石蕊试纸变红的气体,则原溶液中一定含有${NH}_{4}^{+}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 单质熔、沸点逐渐降低 | B. | 单质的氧化性逐渐增强 | ||
| C. | 气态氢化物沸点逐渐升高 | D. | 气态氢化物稳定性逐渐减弱 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com