
【题目】4,7二甲基香豆素(熔点:132.6 ℃)是一种重要的香料,广泛分布于植物界中,由间甲基苯酚为原料的合成反应如下:
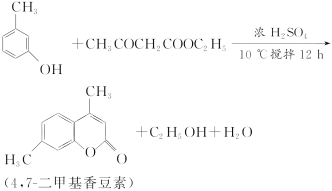
实验装置图如下:

主要实验步骤:
步骤1:向装置a中加入60 mL浓硫酸,并冷却至0 ℃以下,搅拌下滴入间甲基苯酚30 mL(0.29 mol)和乙酰乙酸乙酯26.4 mL(0.21 mol)的混合物。
步骤2:保持在10 ℃下,搅拌12 h,反应完全后,将其倒入冰水混合物中,然后抽滤、水洗得粗产品。
步骤3:粗产品用乙醇溶解并重结晶,得白色针状晶体并烘干,称得产品质量为33.0 g。
(1)简述装置b中将活塞上下部分连通的目的________________________。
(2)浓H2SO4需要冷却至0 ℃以下的原因是__________________________。
(3)反应需要搅拌12 h,其原因是_________________________________。
(4)本次实验产率为________。(百分数保留一位小数)
(5)实验室制备乙酸乙酯的化学反应方程式:_____________________________,用________(填药品名称)收集粗产品,用________(填操作名称)的方法把粗产品分离。
【答案】(1)平衡上下气压,使漏斗中液体顺利流下
(2)防止浓H2SO4将有机物氧化或炭化
(3)使反应物充分接触反应,提高反应产率 (4)90.3%
(5)CH3CH2OH+CH3COOH![]() CH3COOCH2CH3+H2O 饱和碳酸钠溶液 分液
CH3COOCH2CH3+H2O 饱和碳酸钠溶液 分液
【解析】(1)装置b中将活塞上下部分连通的目的是平衡上下气压,使漏斗中液体顺利流下。(2)浓硫酸具有强氧化性和脱水性,因此浓H2SO4需要冷却至0 ℃以下的原因是防止浓H2SO4将有机物氧化或炭化。(3)搅拌可以使反应物充分接触反应,提高反应产率。(4)反应中间甲基苯酚是0.29 mol,乙酰乙酸乙酯是0.21 mol,所以根据方程式可知理论上应该生成0.21 mol 4,7二甲基香豆素,质量是0.21 mol×174 g·mol-1=36.54 g。实际生产中得到4,7二甲基香豆素的质量是33.0 g,所以本次实验产率为![]() ×100%=90.3%。(5)实验室制备乙酸乙酯的化学反应方程式为CH3CH2OH+CH3COOH
×100%=90.3%。(5)实验室制备乙酸乙酯的化学反应方程式为CH3CH2OH+CH3COOH![]() CH3COOCH2CH3+H2O,用饱和碳酸钠溶液收集粗产品,由于乙酸乙酯难溶于水,所以用分液的方法把粗产品分离。
CH3COOCH2CH3+H2O,用饱和碳酸钠溶液收集粗产品,由于乙酸乙酯难溶于水,所以用分液的方法把粗产品分离。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】联氨(又称联肼,N2H4,无色液体)是一种应用广泛的化工原料,可用作火箭燃料,回答下列问题:
(1)联氨分子的电子式为_____________,其中氮的化合价为______________。
(2)实验室可用次氯酸钠溶液与氨反应制备联氨,反应的化学方程式为___________。
(3)①2O2(g)+N2(g)=N2O4(l)△H1
②N2(g)+2H2(g)=N2H4(l)△H2
③O2(g)+2H2(g)=2H2O(g)△H3
④2N2H4(l)+N2O4(l)=3N2(g)+4H2O(g)△H4=-1048.9kJ/mol
上述反应热效应之间的关系式为△H4=____________,联氨和N2O4可作为火箭推进剂的主要原因为________________。
(4)联氨为二元弱碱,在水中的电离方程式与氨相似。联氨与硫酸形成的酸式盐的化学式为 。
(5)联氨是一种常用的还原剂,可用于处理高压锅炉水中的氧,防止锅炉被腐蚀。理论上1kg的联氨可除去水中溶解的O2 kg;与使用Na2SO3处理水中溶解的O2相比,联氨的优点是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A. 所有金属元素都分布在d区和ds区
B. 最外层电子数为2的元素都分布在s区
C. 元素周期表中ⅢB族到ⅡB族10个纵列的元素都是金属元素
D. s区均为金属元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一个密闭绝热容器(W)中,进行如下两个可逆反应:①A(g)+2B(g)![]() 3C(g)+D(s)△H1>0,②xM(g)+N(g)
3C(g)+D(s)△H1>0,②xM(g)+N(g)![]() 3Q(g)△H2.反应①中各物质与反应②中各物质均不发生反应. M的转化率与温度、压强的关系如图所示.
3Q(g)△H2.反应①中各物质与反应②中各物质均不发生反应. M的转化率与温度、压强的关系如图所示.
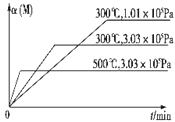
下列对W容器中进行的反应推断合理的是( )
A.x=2
B.平衡时, v 正 (B):v 逆 (C)=2:3
C.若保持容器容积不变,充入N,则C的物质的量减小
D. 若保持容器容积不变,充入Q,反应①的平衡常数不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了除去MgCl2溶液中的FeCl3,可在加热搅拌的条件下加入一种试剂,该试剂是( )
A. NaOH B. MgO C. 氨水 D. Na2CO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图为一种天然产物,具有一定的除草功效。下列有关该化合物的说法错误的是( )
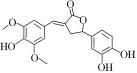
A.分子中含有三种含氧官能团
B.1 mol该化合物最多能与4 mol NaOH反应
C.既可以发生取代反应,又能够发生加成反应
D.既能与FeCl3发生显色反应,也能和NaHCO3反应放出CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组用0.50 mol·L-1 NaOH溶液和0.50 mol·L-1硫酸溶液进行中和热的测定。
Ⅰ.配制0.50 mol·L-1 NaOH溶液
(1)若实验中大约要使用245 mL NaOH溶液,至少需要称量NaOH固体________g。
(2)从下图中选择称量NaOH固体所需要的仪器(填字母):__________ 。
名称 | 托盘天平(带砝码) | 小烧杯 | 坩埚钳 | 玻璃棒 | 药匙 | 量筒 |
仪器 |
|
|
|
|
|
|
序号 | a | b | c | d | e | f |
Ⅱ.测定稀硫酸和稀氢氧化钠中和热的实验装置如下图所示。
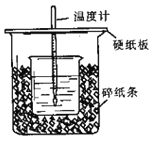
(1)此装置哪些地方需要改进:________________
(2)写出该反应的中和热的热化学方程式(中和热为57.3 kJ·mol-1):__________________
(3
起始温度/℃ | 终止温度/℃ | 温度差/℃ | |||
H2SO4 | NaOH | 平均值 | |||
1 | 25.5 | 25.0 | 25.25 | 28.5 | 3.25 |
2 | 24.5 | 24.2 | 24.35 | 27.6 | 3.25 |
3 | 25.0 | 24.5 | 24.75 | 26.5 | 1.75 |
①近似认为0.50 mol·L-1 NaOH溶液和0.50 mol·L-1硫酸溶液的密度都是1 g·cm-3,中和后生成溶液的比热容c=4.18 J·g-1·℃-1。则中和热ΔH=_______________(取小数点后一位)。
②上述实验数值结果与57.3 kJ·mol-1有偏差,产生偏差的原因可能是(填字母)____________。
a.实验装置保温、隔热效果差
b.量取NaOH溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
(4)如果用50 mL 0.55 mol·L-1的氨水代替NaOH溶液进行上述实验,其放出的热量偏小,原因是________________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com