
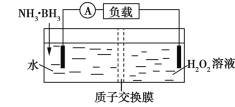
【题目】氨硼烷(NH3·BH3)电池可在常温下工作,装置如图所示。未加入氨硼烷之前,两极室质量相等,电池反应为NH3·BH3+3H2O2═NH4BO2+4H2O。已知两极室中电解质足量,下列说法正确的是
A. 正极的电极反应式为2H++2![]() ═H2↑
═H2↑
B. 电池工作时,H+通过质子交换膜向负极移动
C. 电池工作时,正、负极分别放出H2和NH3
D. 工作一段时间后,若左右两极室质量差为1.9 g,则电路中转移0.6 mol电子
【答案】D
【解析】
本题考察新型原电池工作原理,根据电池反应可知,正、负极的电极反应分别为
3H2O2+6H++6e-=6H2O、NH3·BH3+2H2O-6e-=NH4BO2+6H+。
A. 正极的电极反应式为:3H2O2+6H++6e-=6H2O,没有气体生成,A项错误;
B.原电池工作时,氢离子作为阳离子向正极移动,B项错误;
C.两电极反应分别为:3H2O2+6H++6e-=6H2O、NH3·BH3+2H2O-6e-=NH4BO2+6H+。
两极均没有气体生成,C项错误;
D.从电极反应式来看,如有6mol电子转移,则左极室质量增加31g-6g=25g,右极室质量增加6g,两极室质量之差为19g,所以当左右两室质量差为1.9g时,电路中转移0.6mol电子,D项正确;
所以答案选择D项。


科目:高中化学 来源: 题型:
【题目】NA表示阿伏加德罗常数的值, 下列叙述正确的是
A. 1mol H2O中含有的极性共价键数目为2NA
B. 16 g16O2和18O2混合物中含有的质子数目为8NA
C. Zn和浓硫酸反应得到22.4LSO2和 H2混合气体时, 转移的电子数为4NA
D. 标准状况下2 mol NO与1 mol O2充分反应后分子数共2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ba(NO3)2可用于生产烟花。某主要生产BaCl2、BaCO3、BaSO4的化工厂利用某种钡泥[主要含有BaCO3、Ba(FeO2)2、极少量CuCO3等]制取Ba(NO3)2晶体,其部分工艺流程如下:
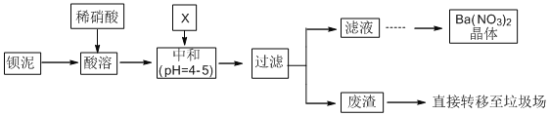
已知:Fe3+和Fe2+以氢氧化物形式沉淀完全时,溶液的pH分别为3.2和9.7。
(1)酸溶时不使用浓硝酸的原因是_________________________________。
(2)酸溶后溶液中pH=1,Ba(FeO2)2与HNO3的反应化学方程式为__________________。
(3)该厂结合本厂实际,中和选用的X为____________(填化学式);中和使溶液中______(填离子符号)的浓度减少(中和引起的溶液体积变化可忽略)。
(4)滤液得到Ba(NO3)2晶体的操作依次为_________、_________、过滤。
(5)该厂生产的Ba(NO3)2晶体含有少量Cu2+。化学上通过惰性电极电解法富集Cu时,发现电解装置的阴极还有少量使红色石蕊试纸变蓝的气体生成。生成该气体的电极反应为______________________________。
(6)Ba2+致死量为355mg/kg。误食Ba2+可以服用MgSO4溶液解毒,涉及到的离子反应方程式为___________;为了减少环境污染,请对上述流程中不合理的设计进行改进,改进措施是__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,对于A2(g)+3B2(g)![]() 2AB3(g)反应来说,下列所表示的化学反应速率中最大的是
2AB3(g)反应来说,下列所表示的化学反应速率中最大的是
A. v(A2)=0.8mol·L-1·s-1 B. v(A2)=40mol·L-1·min-1
C. v(AB3)=1.0mol·L-1·s-1 D. v(B2)=1.2mol·L-1·s-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25 °C时某些弱酸的电离平衡常数如下表,下列说法正确的是
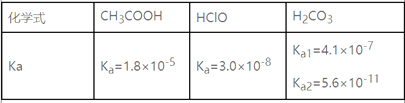
A. 等物质的量浓度溶液酸性由强到弱的顺序为:H2CO3>CH3COOH>HClO
B. 向次氯酸钠溶液中通入少量二氧化碳气体的离子方程式为:ClO-+CO2+H2O=CO32-+2HClO
C. 等物质的量浓度的NaClO和NaHCO3 混合溶液中:c(HClO)+c(ClO-)=c(HCO3-)+c(CO32-)+c(H2CO3)
D. 等pH情况下,溶液的物质的量浓度由大到小的顺序为:Na2 CO3>NaClO>NaHCO3>CH3COONa
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中不正确的是
A.从1 L 1 mol·L-1的NaCl溶液中取出10 mL,其浓度仍是1 mol·L-1
B.配制0.5 L 10 mol·L-1的盐酸,需要氯化氢气体112 L(标准状况)
C.0.5 L 2 mol·L-1BaCl2溶液中,Ba2+和Cl-总数为3×6.02×1023
D.10 g 98%的硫酸(密度为1.84 g· cm-3)与10 mL 18.4 mol·L-1硫酸的浓度是不同的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(题文)(题文)PHB塑料是一种在微生物作用下可降解成无机物的环保型塑料,工业上可用异戊二烯合成:

已知:

(—R1、—R2、—R3、—R均为烃基)
请回答下列问题:
(1)A用系统命名法命名为_____,D中官能团的名称是_______。
(2)反应①的反应类型为_______________。
(3)B与H2反应后的产物的结构简式为![]() ,则B的结构简式为_____。
,则B的结构简式为_____。
(4)写出反应④的化学方程式:_________________________________。
(5)C的同分异构体X满足下列条件:
①能发生水解反应和银镜反应;②1个分子中含有2个碳氧双键。则符合条件的X共有______种。
另一种同分异构体Y能与碳酸钠溶液反应放出气体,能发生银镜反应,核磁共振氢谱共有四组峰且峰面积之比为1∶1∶2∶2,则Y的结构简式为_________。
(6)参照PHB的上述合成路线,设计一条由D为起始原料制备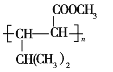 的合成路线(其他试剂任选)______________。
的合成路线(其他试剂任选)______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法或表达式正确的是( )
A. 0.5mol 稀 H2 SO 4与0.5mol 稀 Ba (OH )2溶液反应放出akJ热量,则中和热为 akJ/ mol
B.  则热量变化关系式: △H1+△H3+△H5=-(△H2+△H4)
则热量变化关系式: △H1+△H3+△H5=-(△H2+△H4)
C. △H与反应方程式中的化学计量数,物质的状态和可逆反应均有关
D. 同温同压下, H2( g)+ Cl 2(g)= 2HCl (g)在光照和点燃条件下的△H不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制乙炔的实验中,下列说法错误的是( )
A. 反应的原料之一CaC2,俗称电石,是由焦炭、熟石灰在电炉中高温反应制得
B. 在实验中可用饱和食盐水代替纯水,有利于控制反应速率
C. 该反应原理是:CaC2+2H2O→HC![]() CH
CH![]() +Ca(OH)2
+Ca(OH)2
D. 反应过程中会闻到难闻的气味是因为电石中含有的杂质造成的
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com