

分析 (1)根据盖斯定律可以计算化合反应的焓变,根据反应自发行的判据:△H-T△S<0进行回答;
(2)①反应速率v=$\frac{△c}{△t}$,根据图象可知,在第一个平衡时段的CO的物质的量为0.2mol,则此时生成的H2也是0.2mol,反应体系中水的物质的量为1.2mol,可得知物质的平衡浓度,再根据K=$\frac{c(CO)c({H}_{2})}{c({H}_{2}O)}$计算,
②反应进行至2min时,根据图象知,相同时间内,水和一氧化碳的物质的量变化量大于0-1min内,说明反应速率增大,根据温度对反应速率、化学平衡的移动的影响分析;
③反应至第5min时,CO的物质的量不变,水的物质的量增大,说明改变的量是水的物质的量;
(3)根据反应I、反应III均为放热反应,温度升高不利于CO2、CO转化为甲醇,反应II为吸热反应,温度升高使更多的CO2转化为CO来回答;
(4)该燃料电池中,通入CO的电极为负极,负极上CO失电子和碳酸根离子反应生成二氧化碳和水,通入O2的电极为正极,正极上氧气得电子和二氧化碳反应生成碳酸根离子,根据电子得失守恒计算电解食盐水中产生的氢氧根离子的物质的量,进而确定pH值,据此答题.
解答 解:反应Ⅰ:CO2 (g)+3H2 (g)?CH3OH(g)+H2O(g)△H1=-49.58kJ•mol-1
反应Ⅱ:CO2 (g)+H2 (g)?CO(g)+H2O(g)△H2=+41.19kJ•mol-1
反应Ⅲ:CO(g)+2H2(g)?CH3OH(g)△H3
根据盖斯定律,反应Ⅲ可以是Ⅰ-Ⅱ得到,所以反应Ⅲ的焓变△H2=(-49.58kJ•mol-1)-(+41.19kJ•mol-1)=-90.77kJ•mol-1,根据反应自发行的判据:△H-T△S<0,反应Ⅲ是熵减的放热的反应,所以要自发进行需要在较低温下进行,
故答案为:-90.77kJ•mol-1;较低温;
(2)①根据图象可知,在第一个平衡时段的CO的物质的量为0.2mol,则此时生成的H2也是0.2mol,0~1min 内用H2表示该反应的速率=$\frac{\frac{0.2mol}{2L}}{1min}$=0.1mol•L-1•min-1,反应体系中水的物质的量为1.2mol,容积为2L,所以此时CO的平衡浓度为0.1mol/L,H2的平衡浓度为0.1mol/L,H2O的平衡浓度为0.6mol/L,则K=$\frac{c(CO)c({H}_{2})}{c({H}_{2}O)}$=$\frac{0.1mol/L×0.1mol/L}{0.6mol/L}$=0.017mol•L-1,
故答案为:0.1mol•L-1•min-1;0.017mol•L-1;
②应进行至2min时,根据图象知,相同时间内,水和一氧化碳的物质的量变化量大于0-1min内,说明反应速率增大,水蒸气的物质的量减少,一氧化碳的物质的量增加,说明平衡向正反应方向移动,而该反应为吸热反应,则该改变的条件只能是升高温度,
故答案为:升温;
③反应至第5min时,CO的物质的量不变,水的物质的量增大,说明改变的量是增加水的物质的量,随反应进行水蒸气减小,一氧化碳增大,平衡正向进行;
a、增加了C是固体,不影响化学平衡,故a错误;
b、增加了水蒸气,5min时,CO的物质的量不变,水的物质的量增大,故b正确;
c、反应是吸热反应,降低了温度平衡逆向进行,图象不符合,故c错误;
d、增加了压强,平衡逆向进行,不符合图象变化,故d错误;
故答案为:b;
(3)反应I、反应III均为放热反应,温度升高不利于CO2、CO转化为甲醇,反应II为吸热反应,温度升高使更多的CO2转化为CO,所以当温度高于260℃后,CO的浓度一定增大,
故答案为:增大; 反应Ⅰ、反应Ⅱ均为放热反应,温度升高不利于CO2、CO转化为甲醇;反应Ⅱ为吸热反应,温度升高使更多的CO2转化为CO.综上所述,CO的浓度一定增大;
(4)该燃料电池中,通入CO的电极为负极,负极上CO失电子和碳酸根离子反应生成二氧化碳和水,负极反应式为CO+CO32--2e-=2CO2,当有5.6g(即0.2mol)CO被消耗时,电路中流过的电子的物质的量为0.4mol,根据电解方程式2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑~2e-可知,电解池中产生的氢氧化钠的物质的量为0.4mol,所以氢氧化钠的浓度为$\frac{0.4mol}{0.4L}$=1mol/L,所以溶液的pH=14,
故答案为:CO+CO32--2e-=2CO2;14.
点评 本题考查了热化学方程式、影响化学反应速率和化学平衡移动的因素、电极反应式的书写、电解池的计算等知识点,明确盖斯定律和化学平衡移动原理及电子得失守恒是解题目的关键,题目难度中等.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | MgO和Al2O3在工业上用于制作耐高温材料,也可用于电解法冶炼Mg、Al | |
| B. | 水泥冶金厂常用高压电除去工厂烟尘,利用了胶体的性质 | |
| C. | 高空臭氧层吸收太阳紫外线,保护地球生物;反应3O2═2O3有单质参加,属于氧化还原反应 | |
| D. | 向水中加入明矾进行杀菌消毒 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 族 周期 | I A | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | O |
| 1 | A | |||||||
| 2 | D | E | G | I | ||||
| 3 | B | C | F | H |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
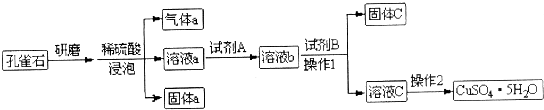
| A. | 研磨孔雀石的目的是增大固体表面积,从而加快反应速率 | |
| B. | 试剂A目的是将溶液中Fe2+转化为Fe3+,可选用双氧水作氧化剂 | |
| C. | 试剂B目的是作pH调节剂,使Fe3+转化为沉淀 | |
| D. | 试剂B可以选择NaOH或氨水等碱性试剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 氢氧化物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 | Mn(OH)2 |
| 开始沉淀的pH | 3.3 | 1.5 | 6.5 | 5.4 | 8.3 |
| 沉淀完全的pH | 5.2 | 3.7 | 9.7 | 6.7 | 9.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 | |
| 第2周期 | ① | ② | ||||||
| 第3周期 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
| 第4周期 | ⑨ | ⑩ |
 ,
,查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
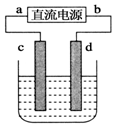 如图,电解质溶液是NaCl的水溶液,过一段时间发现d极附近有黄绿色气体产生,(c、d均为石墨电极)以下说法正确的是( )
如图,电解质溶液是NaCl的水溶液,过一段时间发现d极附近有黄绿色气体产生,(c、d均为石墨电极)以下说法正确的是( )| A. | a是电源的正极 | B. | 电子流动的方向:d→b | ||
| C. | c极发生氧化反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com