
请回答以下问题:
(1)该结晶水合物中含有的两种阳离子是___________和___________,阴离子是___________。
(2)试通过计算确定该结晶水合物的化学式。
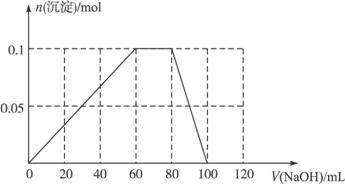
(3)假设该过程中向该溶液中加入的NaOH溶液的物质的量浓度为5 mol·L-1,请在下图中画出生成沉淀的物质的量与加入NaOH溶液体积的关系示意图。
(1) ![]() Al3+
Al3+ ![]()
(2)n(![]() )=
)=![]() =0.2mol
=0.2mol
n(![]() )=
)=![]() =0.1 mol
=0.1 mol
根据离子化合物中阴、阳离子电荷平衡的原理:n(![]() )+3n(Al3+)=2n(
)+3n(Al3+)=2n(![]() )可得:
)可得:
n(Al3+)=![]() (2×0.2 mol-0.1 mol)=0.1 mol?
(2×0.2 mol-0.1 mol)=0.1 mol?
n(H2O)=![]() =1.2 mol
=1.2 mol
该结晶水合物的化学式为NH4 Al (SO4)2·12H2O 〔或(NH4)2SO4·Al2(SO4)3·24H2O〕
(3)?

解析:根据与NaOH、Ba(OH)2反应的现象,可推知该结晶水合物含![]() 、Al3+、
、Al3+、![]() 。
。
据46.6 g BaSO4可计算:n(![]() )=
)=![]() =0.2 mol,
=0.2 mol,
据2.24 L NH3可知n(![]() )=0.1 mol,
)=0.1 mol,
则:n(Al3+)=![]() (2×0.2 mol-0.1 mol)=0.1 mol,
(2×0.2 mol-0.1 mol)=0.1 mol,
n(H2O)=1.2 mol
n(![]() )∶n(Al3+)∶n(
)∶n(Al3+)∶n(![]() )∶n(H2O)=1∶1∶2∶12
)∶n(H2O)=1∶1∶2∶12
故该结晶水合物化学式为NH4Al(SO4)2·12H2O或(NH4)2SO4·Al2(SO4)3·24H2O。
由于加入NaOH时,Al3+先生成沉淀,需n(OH-)=0.3 mol,V(NaOH)=60 mL,
然后![]() 与OH-反应,需n(OH-)=0.1 mol,V(NaOH)=20 mL,
与OH-反应,需n(OH-)=0.1 mol,V(NaOH)=20 mL,
最后Al(OH)3溶解,需n(OH-)=0.1 mol,V(NaOH)=20 mL,
据此可作出图象。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com