
| |||||||||||||||
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
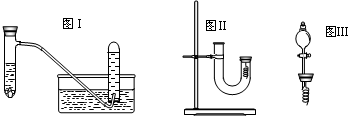
| 实验步骤 | 问题 |
| 1从U型管左端加入稀硝酸直至充满U型管右端 | ∥/ |
| 2用附有铜丝的胶塞塞住U型管右端,观察现象 | 现象是______ |
| 3待反应停止后打开胶塞,观察实验现象 | 现象是______ |
查看答案和解析>>
科目:高中化学 来源:北京期末题 题型:推断题
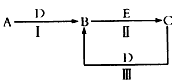
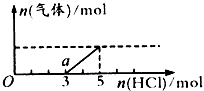
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C是中学常见的无机物,且各由两种元素组成;甲、乙、丙是三种常见的单质;这些化合物和单质间存在如图所示的转化关系(这些转化都不需要使用催化剂)。
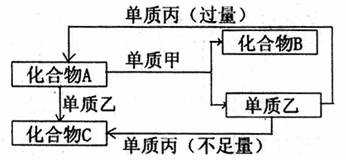
请回答下列问题:
(1)若甲在转化中是还原剂,乙是常见非金属固态单质,且甲、乙、丙都是由短周期元素组成,则:甲 ;乙 ;丙 (填化学式);化合物A的电子式 。A与甲反应的化学方程式为 。
(2)若甲在转化中为氧化剂,是常见非金属气态单质,丙是常见金属,甲、乙、丙中只有甲由短周期元素组成,乙的组成元素与甲的组成元素同主族、与丙的组成元素同周期,乙有强氧化性。且反应均在通常条件下的溶液中进行,则:
① A与乙反应的离子方程式为 ;
②当A与甲的物质的量之比为![]() 时,A与甲恰好完全反应,且符合图中所示的转化关系,则反应的离子方程式为 。
时,A与甲恰好完全反应,且符合图中所示的转化关系,则反应的离子方程式为 。
③0.1mol的单质甲与50mL1.5 mol ? L 1化合物A的溶液反应,则化合物A中被氧化的阴、阳离子的物质的量之比是 。
查看答案和解析>>
科目:高中化学 来源:2010-2011学年江苏省常州市金坛市高一(下)期中化学试卷(解析版) 题型:解答题
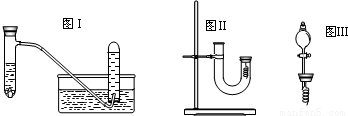
| 实验步骤 | 问题 |
| 1从U型管左端加入稀硝酸直至充满U型管右端 | ∥/ |
| 2用附有铜丝的胶塞塞住U型管右端,观察现象 | 现象是______ |
| 3待反应停止后打开胶塞,观察实验现象 | 现象是______ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com