
【题目】固体碘化铵置于密闭容器中,加热至一定温度后恒温;容器中发生反应:①NH4I(s)![]() NH3(g)+HI(g)②2HI(g)
NH3(g)+HI(g)②2HI(g)![]() H2(g)+I2(g),测得平衡时c(H2)=0.5mol/L,反应①的平衡常数为20,则下列结论正确的是 ( )
H2(g)+I2(g),测得平衡时c(H2)=0.5mol/L,反应①的平衡常数为20,则下列结论正确的是 ( )
A. 平衡时HI分解率为20%
B. 当固体碘化铵物质的量增大一倍,则在相同条件下,容器内压强变大
C. 固体碘化铵一定完全分解
D. 平衡时C(HI)=5mol/L
【答案】A
【解析】设平衡时NH3的浓度为x,HI的浓度为y,由反应①②的关系知,反应②中分解的HI的浓度为0.5×2=1.0mol/L,故反应①中分解产生的HI为(y+1.0)mol/L,此值也等于反应①中分解产生的NH3的浓度,即y+1.0=x;反应①的平衡常数为20,故(x-1)×x=20,故x=5mol/L,据此可求出平衡时C(HI),平衡时HI分解率;该反应为可逆反应,反应物不能消耗完,固体的量增减,对容器内压强无影响;据以上分析解答。
设平衡时NH3的浓度为x,HI的浓度为y,由反应①②的关系知,反应②中分解的HI的浓度为0.5×2=1.0mol/L,故反应①中分解产生的HI为(y+1.0)mol/L,此值也等于反应①中分解产生的NH3的浓度,即y+1.0=x。反应①的平衡常数为20,故(x-1)×x=20,故x=5mol/L,平衡时C(HI)=5-1=4 mol/L,D错误;平衡时HI分解率为2×0.5÷(y+1.0)=1÷5=20%,A正确;增加碘化铵的质量,平衡不动,不影响容器内的压强,B错误;反应①为可逆反应,故固体碘化铵一定不能完全分解,C错误;正确选项A。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】某化学兴趣小组要完成中和热的测定实验.
(1)实验桌上备有烧杯(大、小两个烧杯)、泡沫塑料、泡沫塑料板、胶头滴管、量筒、稀盐酸(0.5molL﹣1)、稀 NaOH溶液(0.55molL﹣1),尚缺少的实验玻璃用品是、 .
(2)写出表示稀盐酸和稀氢氧化钠溶液反应中和热的热化学方程式(中和热为57.3kJmol﹣1): .
(3)若用稀醋酸、稀硫酸、浓硫酸分别和稀氢氧化钠溶液反应来测定中和热,恰好完全反应时对应的热效应分别为△H1、△H2、△H3的大小关系是 .
(4)每组实验所用氢氧化钠溶液和稀盐酸的体积均为 50mL,可近似认为该实验中稀盐酸和稀氢氧化钠溶液的密度均为 1g/cm3,中和后生成溶液的比热容c=4.18J/(g℃),实验中记录数据如表所示,请填写表中空白:
编号 | 起始温度T1/℃ | 终止温度T2/℃ | 平均温度差T2﹣T1/℃ | △H | ||
盐酸 | NaOH | 平均值 | ||||
① | 26.2 | 26.0 | 26.1 | 29.2 |
|
|
② | 25.9 | 25.9 | 25.9 | 29.2 | ||
③ | 26.4 | 26.2 | 26.3 | 29.5 | ||
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在狗年里,人们相互祝愿亲朋好友:狗年旺旺,狗年大发.图是一种形状酷似一条小狗的有机物键线式结构图,化学家将其取名为“doggycene”,下列有关“doggycene”的说法中正确的是( ) 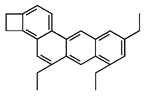
A.该分子中所有碳原子不可能处于同一平面
B.“doggycene”的分子式为C26H30
C.该物质在常温下呈气态
D.1 mol该物质在氧气中完全燃烧生成CO2和H2O的物质的量之比为1:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据报道,法国里昂的科学家最近发现一种只由四个中子构成的粒子,这种粒子称为“四中子”,也有人称之为“零号元素”。下列有关“四中子”粒子的说法不正确的是
A.该粒子不显电性B.该粒子质量比氢原子大
C.该粒子质量数为4D.在周期表中与氢元素占同一位置
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】不符合原子核外电子排布基本规律的是
A.核外电子总是优先排在能量最低的电子层上
B.K层是能量最低的电子层
C.N电子层为次外层时,最多可容纳的电子数为18
D.各电子层(n)最多可容纳的电子数为n2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】烯烃A在一定条件下可以按下面的框图进行反应. 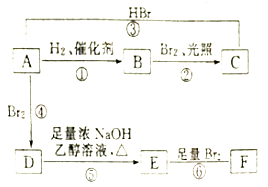
已知:D是 
请填空:
(1)A的结构简式是 .
(2)框图中属于取代反应的是消去反应(填数字代号).
(3)框图中①、③、⑥属于反应.
(4)C的结构简式是 .
(5)写出由D→E的化学方程式;写出由E→F的化学方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO和NO都是汽车尾气中的有害物质,它们之间能缓慢地发生如下反应:2NO(g)+2CO(g) ![]() N2(g)+2CO2(g) ΔH<0,现利用此反应,拟设计一种环保装置,用来消除汽车尾气对大气的污染,下列设计方案可以最有效的提高尾气处理效果的是 ( )
N2(g)+2CO2(g) ΔH<0,现利用此反应,拟设计一种环保装置,用来消除汽车尾气对大气的污染,下列设计方案可以最有效的提高尾气处理效果的是 ( )
①选用适当的催化剂 ②提高装置温度 ③降低装置的压强 ④装置中放入碱石灰
A. ①④ B. ②④ C. ① D. ②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铵明矾[NH4Al(SO4)2·12H2O]是分析化学常用的基准试剂,工业上常用铝土矿(主要成分为Al2O3)来生产铵明矾,其中Z的水溶液可用于伤口消毒,其工艺流程图如下:
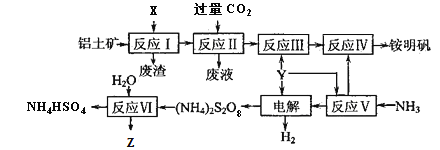
(1)写出反应Ⅱ的离子方程式____________________。
(2)25℃时,将0.2 mol·L-1的氨水与0.1 mol·L-1的Y溶液等体积混合,所得溶液的pH=5,则该温度下氨水的电离常数Kb≈_____________(忽略混合时溶液体积的变化)。
(3)从反应Ⅳ的铵明矾溶液中获得铵明矾晶体的实验操作依次为_____________、____________、过滤、洗涤(填操作名称)。
(4)“电解”时,用惰性材料作电极,则阳极电极反应式为__________________________。
(5)反应Ⅵ的化学方程式为______________________。
(6)废水中含有Fe2+、Mn2+等金属离子对自然环境有严重的破坏作用,,可用(NH4)2S2O8氧化除去。写出Mn2+被氧化生成MnO2的离子方程式为__________________________________。Z也有较强氧化性,在实际生产中不用Z氧化Mn2+的原因是_______________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com