
(7分)(1)室温下,将1g苯(C6H6)完全燃烧生成液态水和CO2,放出41.8kJ的热量,写出C6H6燃烧的热化学方程式 。
(2)今有两个氢气燃烧生成水的热化学方程式
H2(g)+1/2O2(g) ==H2O(g) △H=a kJ/mol
2H2(g)+O2(g) ==2H2O(l) △H=b kJ/mol
请回答下列问题:(提示:b表示b的绝对值)
①若2 molH2完全燃烧生成水蒸气,则放出的热量 (填“>”、“<”或“=”)bkJ
②反应热的关系:2a b(填“>”、“<”或“=”)。
③ 若已知H2(g)+1/2O2(g) ==H2O(g) △H=―242 kJ/mol ,且氧气中1mol氧氧键完全断裂时吸收热量496kJ,水蒸气中1molH―O键形成时放出热量463kJ,则氢气中1molH―H键断裂时吸收的热量为 一本好题口算题卡系列答案
一本好题口算题卡系列答案科目:高中化学 来源: 题型:阅读理解
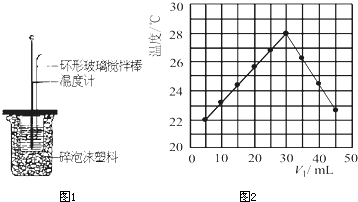
| 温度 | 起始温度t1/℃ | 终止温度 t1/℃ |
温度差 (t2-t1)t1/℃ | ||
| 实验次数 | H2SO4 | NaOH | 平均值 | ||
| 1 | 26.2 | 26.0 | 26.1 | 30.1 | 4.0 4.0 |
| 2 | 27.0 | 27.4 | 27.2 | 33.3 | |
| 3 | 25.9 | 25.9 | 25.9 | 29.8 | |
| 4 | 26.4 | 26.2 | 26.3 | 30.4 | |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
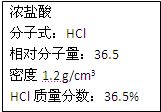 右图为实验室某浓盐酸试剂瓶上的标签,试根据有关数据回答下列问题:
右图为实验室某浓盐酸试剂瓶上的标签,试根据有关数据回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 右图为实验室某浓盐酸试剂瓶上的标签,试根据有关数据回答下列问题:
右图为实验室某浓盐酸试剂瓶上的标签,试根据有关数据回答下列问题:查看答案和解析>>
科目:高中化学 来源:同步题 题型:实验题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com