
����Ŀ��ij��ѧС��ͬѧ������װ�ú��Լ�����ʵ�飬̽��O2��KI��Һ������Ӧ��������
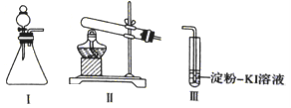
��ѡ�Լ���30%H2O2��Һ��0.lmol/LH2SO4��Һ��MnO2���塢KMnO4����
��1��С��ͬѧ��Ƽס��ҡ�������ʵ�飬��¼����
���� | ���� | |
�� | ��I����ƿ�м���_____����I��_________�м���30%H2O2��Һ������I��. �������� | I�в�����ɫ���岢�����������������������ð������ҺѸ�ٱ��� |
�� | �����м���KMnO4���壬��������������ȼ�ƾ��� | ����������ð������Һ������ |
�� | �����м���KMnO4���壬���м�������0.1 mol/L H2SO4��Һ����������������ȼ�ƾ��� | ����������ð������Һ���� |
��2����ʵ����O2��KI��Һ��Ӧ�����ӷ���ʽ��___________________________��
��3���Ա��ҡ���ʵ���֪��O2��KI��Һ������Ӧ������������__________________��Ϊ��һ��̽���������Է�Ӧ���ʵ�Ӱ�죬�ɲ�ȡ��ʵ���ʩ��___________________________��
��4���ɼס��ҡ�����ʵ���Ʋ⣬��ʵ�������I�еİ���ʹ��Һ������ѧ����I�в���������ֱ��ͨ������__________ ������ĸ����Һ��֤���˰����к���H2O2��
A.���� KMnO4 B. FeC12 C. Na2S D.Ʒ��
��5��������ʾ��KI��Һ�ڿ����о��ù����лᱻ����������4KI+O2+2H2O==2I2+4KOH����С��ͬѧȡ20 mL���õ�KI��Һ�������м��뼸�ε�����Һ�����û�й۲쵽��Һ��ɫ���������Dz�������Ƿ����˷�Ӧ��3I2+6OH-==5I-+IO3-+3H2O��ɵġ������ʵ��֤�����ǵIJ����Ƿ���ȷ��________________________________��
���𰸡� MnO2���� ��Һ©�� O2+4I-+4H+==2I2+2H2O ���Ի��� ʹ�ò�ͬŨ�ȵ�ϡ�������Ա�ʵ�� AD ������δ��������Һ�е���0.1mol/LH2SO4��Һ���۲���������Һ�������������ȷ���������
��������(1)��ʵ�飺����װ�â���Ҫ������ȡ������֪���õ���˫��ˮ�ķֽ⣬���������ڶ������̴������·ֽ�������������I����ƿ�м���MnO2���壬��I�ķ�Һ©���м���30%H2O2��Һ������I��������I�в�����ɫ���岢�����������������������ð������ҺѸ�ٱ���˵�����ɵⵥ�ʣ��ʴ�Ϊ��MnO2���壻��Һ©����
(2)�����Ӿ��л�ԭ�ԣ��������������ܹ������������ɵⵥ�ʣ��ݴ�д����Ӧ�����ӷ���ʽΪ��O2+4I-+4H+=2I2+2H2O���ʴ�Ϊ��O2+4I-+4H+=2I2+2H2O��
(3)����м���KMnO4���壬���Ӣ�����ȼ�ƾ��ƣ�����������ð������Һ������������м���KMnO4���壬���м�������0.1mol/LH2SO4��Һ�����Ӣ�����ȼ�ƾ��ƣ�����������ð������Һ�����Ա��ҡ���ʵ���֪��O2��KI��Һ������Ӧ�����������ǣ����Ի�����Ϊ��һ��̽���������Է�Ӧ���ʵ�Ӱ�죬�ɲ�ȡ��ʵ���ʩ�ǣ�ʹ�ò�ͬŨ�ȵ�ϡ�������Ա�ʵ�飬�ʴ�Ϊ�����Ի�����ʹ�ò�ͬŨ�ȵ�ϡ�������Ա�ʵ�飻
(4)A��KMnO4�����������Һ�ܹ���˫��ˮ���������¸��������Һ��ɫ��������������������Һ��Ӧ��������������Һ��ɫ��֤����������к���˫��ˮ����A��ȷ��B��FeCl2���������������Һ���ܹ������������ӣ���֤����������к���˫��ˮ����B����C��Na2S��������غ��������ܹ��������ƣ��������Ƽ������������Ƿ���˫��ˮ����C����D��Ʒ��������������ᱻ������ɫ��ȥ��֤����������к���˫��ˮ����D��ȷ���ʴ�Ϊ��AD��
(5)KI��Һ�ڿ����о��ù����лᱻ����������4KI+O2+2H2O=2I2+4KOH����С��ͬѧȡ20mL���õ�KI��Һ�������м��뼸�ε�����Һ�����û�й۲쵽��Һ��ɫ���������Dz�������Ƿ����˷�Ӧ�����ӷ���ʽΪ��3I2+6OH-=5I-+IO3-+3H2O�����ʵ��֤�����ǵIJ����Ƿ���ȷ���·���Ϊ��������δ��������Һ�е���0.1mol/LH2SO4��Һ�۲���������Һ�����������ȷ��������ʴ�Ϊ��������δ��������Һ�е���0.1mol/LH2SO4��Һ�۲���������Һ�����������ȷ���������


 �ŵ������ϵ�д�
�ŵ������ϵ�д� 53������ϵ�д�
53������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25��ʱ��ˮ�ĵ���ﵽƽ�⣺H2O![]() H++OH-����H>0������������ȷ���ǣ� ��
H++OH-����H>0������������ȷ���ǣ� ��
A. ��ˮ�м���ϡ��ˮ��ƽ�������ƶ���c(OH-)����
B. ��ˮ�м������������������ƣ�c(H+)����Kw����
C. ��ˮ�м�����������CH3COONa��ƽ�������ƶ���c(H+)����
D. ��ˮ���ȣ�Kw���䣬pH����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ṹ�У������ڵ�˫������ṹ������Ϊ֤�ݵ���ʵ��
�ٱ�����ʹ���Ը��������Һ��ɫ
�ڱ�����һ�������¸����������ӳɷ�Ӧ���ɻ�����
�۾�ʵ�����ڶ��ױ�(![]() )ֻ��һ�ֽṹ
)ֻ��һ�ֽṹ
�ܱ���FeBr3������ͬҺ��ɷ���ȡ����Ӧ����������ˮ��ɫ
A. �ڢۢ� B. �٢ڢ� C. �٢ۢ� D. �٢ڢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��������Ϊ�������Դ�����ʼ��ٻ�����Ⱦ�����ѳ����ȼ�ͼ״�����ɲ�ҵ��������Ҫ�������£�

��1��д�����ʳ��ˮ��Ӧ�����ӷ���ʽ_______________________________________��
��2��д���������Ȼ����õ����Ȼ��ѵĻ�ѧ����ʽ��___________________________
��3����֪����Mg��s��+Cl2��g��=MgCl2��s������H=��641kJmol��1
��Ti��s��+2Cl2��g��=TiCl4��s������H=��770kJmol��1
��2Mg��s��+TiCl4��g��=2MgCl2��s��+Ti��s������H��=____________________
��Ӧ2Mg+TiCl4![]() 2MgCl4+Ti��Ar�����н��е�������____________________��
2MgCl4+Ti��Ar������������____________________��
��4����������ҵ���У��ϳ�192t�״�����������ⲹ��H2______t���������������������ʵ��κ���ʧ����
��5���Լ״�������������������ҺΪԭ�ϣ�ʯīΪ�缫�ɹ���ȼ�ϵ�أ��õ���и����ϵĵ缫��Ӧʽ��___________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�����廯����C8H6O2�����ķ��ӣ��������ⲻ�������������������У� ��
A. �����ǻ� B. һ��ȩ����һ�ʻ� C. ����ȩ�� D. һ���Ȼ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����4mol A�����2mol B������2L�̶�����������л�ϣ�����һ�������·������·�Ӧ��2A��g��+B��g��2C��g��������2s����C��Ũ��Ϊ0.6molL��1 �� �������м���˵����������ȷ���ǣ� ��
A.������A��ʾ�ķ�Ӧ��ƽ������Ϊ0.6 mol?��L?s����1
B.2 sʱ����B��Ũ��Ϊ1.4 mol?L��1
C.2 sʱ����A��ת����Ϊ70%
D.2 sʱ����A���������Ϊ ![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ�������ļ���ȼ�պ�IJ���ΪCO��CO2��ˮ�������˻����������Ϊ99.2g�����仺��������ˮCaCl2ʱ��CaCl2����50.4g��ԭ���������CO������Ϊ�� ��
A.13.2 g
B.22.4g
C.24.4g
D.26.4g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ṩ�����ƶ�Ԫ�أ�����Ҫ����գ�
��1��ԭ�Ӻ�����3�����Ӳ㣬��۵�����Ϊ7������������Ӧˮ���ﻯѧʽ �� �䵥����NaOH��Ӧ�Ļ�ѧ����ʽΪ ��
��2����֪X+��Y2+��Z����W2���������Ӿ�������ͬ�ĵ��Ӳ�ṹ����X��Y��Z��W������Ԫ�ص�ԭ�������ɴ�С��˳���� �� ԭ�Ӱ뾶�ɴ�С��˳���� ��
��3��A+��B����C��D �������ӣ����ӻ����ӣ������Ƕ��ֱ�10�����ӣ���֪����������ת����ϵ��A++B�� ![]() C+D��������A+��B���ĵ���ʽ���Ƚ�C��D���ȶ��Ե�ǿ����С���û�ѧʽ��ʾ��
C+D��������A+��B���ĵ���ʽ���Ƚ�C��D���ȶ��Ե�ǿ����С���û�ѧʽ��ʾ��
��4����NH4NO3 ��NaF ��CO2 ��K2O2 ��NaOH ��CH4ֻ���м��Լ����� �� �������Ӽ����зǼ��Լ��������������Ӽ����м��Լ����� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ʲ���ͨ�����Ϸ�Ӧ�õ�����
A. Fe(OH)2 B. Fe(OH)3 C. FeCl2 D. FeCl3
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com