


 全能练考卷系列答案
全能练考卷系列答案 一课一练课时达标系列答案
一课一练课时达标系列答案科目:高中化学 来源: 题型:
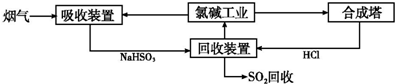
| 分析推测 | 实验步骤及现象 |
| 甲:生成了Fe(OH)3胶体 乙:经查阅资料,可能发生反 应:Fe3++6SO2?Fe(SO2)63+(反应b) | ⅰ.制备Fe(OH)3胶体并检验 ⅱ.分别向Fe(OH)3胶体和该红褐色液体中加入适量铁粉,振荡后前者不变色,后者变为浅绿色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Fe+CuSO4═FeSO4+Cu | ||||
| B、AgNO3+NaCl═AgCl↓+NaNO3 | ||||
C、Fe2O3+3CO
| ||||
D、2KMnO4
|
查看答案和解析>>
科目:高中化学 来源: 题型:
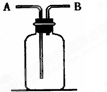 如图所示装置有多种用途,请回答下列问题:
如图所示装置有多种用途,请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| 步骤 | 实验操作 | 实验现象 | 分步推断 |
| (1) | 将取出的2种溶液进行混合 | 混合溶液无色、澄清 无其他明显现象 | 混合溶液中肯定不含Cu(NO3)2 混合溶液肯定不是下列组合: |
| (2) | 用pH试纸测定混合溶液的pH | 测定结果:pH=2 | |
| (3) | 向混合溶液中滴入足量Ba(NO3)2溶液 | 有白色沉淀出现 | |
| (4) | 向上述溶液过滤所得的滤液中滴加AgNO3 | 无明显现象 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2Na+2H2O=2NaOH+H2↑ | ||||
B、C+H2O(g)
| ||||
| C、2F2+2H2O=4HF+O2 | ||||
| D、3NO2+H2O=2HNO3+NO |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Al2(SO4)3 |
| B、NaOH |
| C、BaCl2 |
| D、FeCl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
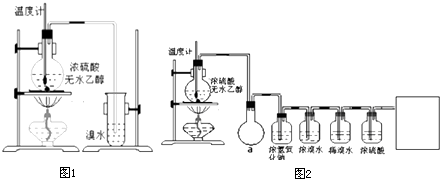
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com