
| A���٣��ڣ��ܣ��� |
| B���ڣ��ۣ��ܣ��� |
| C���٣��ڣ��ۣ��� |
| D���ۣ��ڣ��ܣ��� |


 ���Ǽ���С����ϵ�д�
���Ǽ���С����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��ͼ��ʾ��������A��B�зֱ�װ��20���ˮ50mL���Թ�C��D����ͨ�����д�������ƽ�⣺2NO2��g��?N2O4��g����H=-57kJ/mol������A�м���2g������ʱ��
��ͼ��ʾ��������A��B�зֱ�װ��20���ˮ50mL���Թ�C��D����ͨ�����д�������ƽ�⣺2NO2��g��?N2O4��g����H=-57kJ/mol������A�м���2g������ʱ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��H+��C1-��CO32-��K+ |
| B��NH4+��OH-��Cl-��Na+ |
| C��Na+��NO3-��C1-��K+ |
| D��Ag+��NO3-��Cl-��K+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����V1��V2��c1=c2������Һ��pH��7 |
| B���������Һ��pH=7����c1V1��c2V2 |
| C����c1=c2�����Һ��c��NH4+���Tc��Cl-������V1��V2 |
| D���������Һ��pH��7������Һ��c��NH4+����c��OH-����c��Cl-����c��H+�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��������ӦΪ��O2+2H2O+4e-=4OH- |
| B����ͭӦ��������ͨH2��һ������ |
| C���ŵ�ʱCO32- �������ƶ� |
| D����������ת����Ϊ100%������в���1 mol ˮ�������ɵô�ͭ64g |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��1mol | B��2mol |
| C��2.5mol | D��3mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���������е�ʯī�缫 |
| B����ֹ�������й�ĵ��Һ��ʴ������Ʒ |
| C�����õ����ǵĽ������� |
| D����ֹ����й����Ӻ�Ǧ���ؽ������Ӷ�������ˮԴ����Ⱦ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
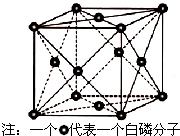 VA��ĵ����ס��飨As����Ԫ�صĻ������ڿ��к���������������Ҫ��;����ش��������⣮
VA��ĵ����ס��飨As����Ԫ�صĻ������ڿ��к���������������Ҫ��;����ش��������⣮�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com