
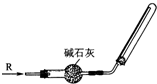
| A. | SO2 | B. | NH3 | C. | CO2 | D. | Cl2 |
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 反应中SO2不能全部转化为SO3 | |
| B. | 无限增加反应时间,SO2能全部转化为SO3 | |
| C. | 达到化学平衡时,反应混合物中同时存在SO2、O2、SO3 | |
| D. | 达到化学平衡时,SO3的生成速率等于SO3的分解速率 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 葡萄糖和福尔马林(含甲醛)与新制氢氧化铜悬浊液共热,都产生砖红色沉淀 | |
| B. | 活性炭和SO2均能使品红溶液褪色 | |
| C. | 在苯、CCl4中加入溴水振荡静置后,溴水层的颜色均变浅或褪去 | |
| D. | 金属钠遇水和乙醇,均能产生氢气 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原溶液中,H2SO4和NaOH的质量 | B. | 原溶液中,H2SO4和NaOH的物质的量 | ||
| C. | 原溶液中,H+和OH-的物质的量 | D. | 原溶液中,H+和OH-的物质的量浓度 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①④ | B. | ③ | C. | ③④ | D. | ②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 江河入海口三角洲的形成通常与胶体的性质有关 | |
| B. | 明矾净水过程中涉及化学变化 | |
| C. | Fe(OH)3胶体与食盐溶液混合将产生聚沉观象 | |
| D. | 沸水中滴加适量饱和FeCl3溶液,可形成带正电荷的胶体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com