A+、B-、C、D、E+五种微粒均含有氢原子,溶液中的A+和B-在加热时相互反应可转化为C和D;B-和E+发生如下反应B-+E+=2D,问:
(1)A+、B-、E+的电子式分别为A+______;B-______;E+______.C、D的化学式分别为:C______、D______.
(2)写出A+与B-在加热时反应的化学方程式______.
(3)C、D、E+的空间构型分别为______、______、______.
(4)以上五种微粒中含有配位键的是:______和______;A+中心原子的杂化方式是______杂化.
解:A
+、B
-、C、D、E
+五种微粒均含有氢原子,溶液中的A
+和B
-在加热时相互反应可转化为C和D,则A
+为NH
4+,B
-为OH
-,B
-+E
+=2D,E
+为H
3O
+,所以D为H
2O,C为NH
3,
(1)A
+、B
-、E
+的电子式分别为
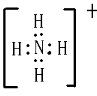
、
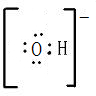
、
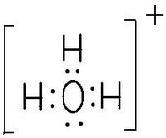
,C为NH
3,D为H
2O,
故答案为:
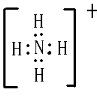
;
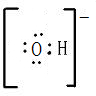
;
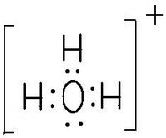
;NH
3;H
2O;
(2)反应生成氨气和水,反应的化学方程式为NH
4++OH
-
NH
3↑+H
2O,故答案为:NH
4++OH
-
NH
3↑+H
2O;
(3)氨气为三角锥型,水为V型,H
3O
+与氨气为等电子体,也为三角锥型,故答案为:三角锥;V型;三角锥;
(4)铵根离子、水合氢离子中氢离子提高空轨道,N或O提供孤对电子形成配位键,NH
4+为正四面体结构,与甲烷相似,中心原子采取sp
3杂化,
故答案为:NH
4+;H
3O
+;sp
3.
分析:A
+、B
-、C、D、E
+五种微粒均含有氢原子,溶液中的A
+和B
-在加热时相互反应可转化为C和D,则A
+为NH
4+,B
-为OH
-,B
-+E
+=2D,E
+为H
3O
+,所以D为H
2O,C为NH
3,
(1)阴阳离子的电子数注意电荷和[];
(2)反应生成氨气和水;
(3)氨气为三角锥型,水为V型,H
3O
+与氨气为等电子体,也为三角锥型;
(4)铵根离子、水合氢离子中氢离子提高空轨道形成配位键,NH
4+为正四面体结构,与甲烷相似.
点评:本题考查常见的10电子微粒,利用反应推断出微粒是解答本题的关键,然后熟悉化学用语及微粒的结构即可解答,题目难度中等.

 、
、 、
、 ,C为NH3,D为H2O,
,C为NH3,D为H2O, ;
; ;
; ;NH3;H2O;
;NH3;H2O; NH3↑+H2O,故答案为:NH4++OH-
NH3↑+H2O,故答案为:NH4++OH- NH3↑+H2O;
NH3↑+H2O;

 A、B、C、D、E五种物质都含1~18号元素中的某 一 元素,它们按图所示关系相互转化,已知A为单质.
A、B、C、D、E五种物质都含1~18号元素中的某 一 元素,它们按图所示关系相互转化,已知A为单质.

