
【题目】用NA表示阿伏加德罗常数的值,下列叙述中正确的是( )
A. 4.0 g H218O中所含电子数为2 NA
B. 0.1 mol H2O2分子中含极性共价键数目为0.3 NA
C. 将含0.1mol FeCl3的饱和溶液滴入沸水中,形成的胶体粒子的数目为0.1NA
D. 含0.2mol H2SO4的浓硫酸与足量铜反应,生成SO2的分子数为0.1NA
 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案科目:高中化学 来源: 题型:
【题目】铝材经脱脂后进行碱洗以除去氧化膜,将碱洗后的溶液中的铝以沉淀形式回收,最好加入下列试剂
A. CO2 B. 氨水 C. NaOH D. HNO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中和热测定实验中,用50mL0.50mol/L盐酸和50mL0.55mol/LNaOH进行实验,下列说法不正确的是( ) 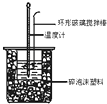
A.改用60mL 0.50mol/L盐酸跟50mL 0.55 mol/L NaOH溶液进行反应,求出的中和热数值和原来相同
B.用50mL0.50mol/L盐酸和50mL0.55mol/LNaOH进行实验比用 50mL0.50mol/L盐酸和50mL0.50mol/LNaOH测得的数值准确
C.酸碱混合时,量筒中NaOH溶液应缓缓倒入小烧杯中,不断用玻璃棒搅拌
D.装置中的大小烧杯之间填满碎泡沫塑料的作用是保温隔热、减少热量损失
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【选修3:物质结构与性质】X、Y、Z、W为原子序数递增的短周期主族元素,R为过渡元素。Y的最高价氧化物的水化物是强酸,Z元素基态原子中有2个未成对电子,基态W原子的价层电子排布式为nsn1npn1 ,X与W为同主族元素。基态的R原子M能层全充满,核外有且仅有1个未成对电子。请回答下列问题:
(1)基态R原子的核外价层电子排布式为____。
(2)X、Y、Z三种元素的第一电离能由大到小的顺序为____(填“元素符号”)。
(3)元素Y的简单气态氢化物的沸点____(高于,低于)元素X的简单气态氢化物的沸点,其主要原因是____,元素Y的简单气态氢化物中Y原子的杂化类型为____,元素X的简单气态氢化物分子的空间构型为____。
(4)Y的气态氢化物在水中可形成氢键,其氢键最可能的形式为____(填字母序号)。
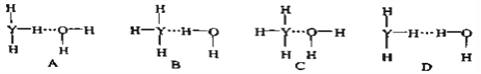
(5)分子中的大π键可用符号Π![]() 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,X的最高价氧化物分子中的大π键应表示为____,其中σ键与π键数目之比为____。
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,X的最高价氧化物分子中的大π键应表示为____,其中σ键与π键数目之比为____。
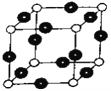
R元素与Y元素形成某种化合物的晶胞结构如图所示(黑球代表R原子),若该晶胞的边长是a cm ,则该晶体的密度为____ g·cm3(用NA表示阿伏伽德罗常数的值)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上制备高纯硅反应的热化学方程式如下:SiCl4(g)+2H2(g)═Si(s)+4HCl(g)△H=+Q kJ/mol(Q>0)某温度、压强下,将一定量反应物通入密闭容器进行以上反应(此条件下为可逆反应),下列叙述中正确的是( )
A.反应过程中,若增大压强能提高SiCl4的转化率
B.若反应开始时SiCl4为1mol,则达平衡时,吸收热量为Q kJ
C.反应至4min时,若HCl浓度为0.12mol/L,则H2的反应速率为0.03mol/(Lmin)
D.当反应吸收热量为0.025QkJ时,生成的HCl通入100mL 1mol/L的NaOH溶液恰好反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分析下图所示的四个装置,其中结论正确的是( )
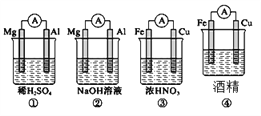
A. ①②中Mg作负极,③④)中Fe作负极
B. ②中Mg作正极,电极反应为6H2O+6e-===6OH-+3H2↑
C. ③中Fe作负极,电极反应为Fe-2e-===Fe2+
D. ④中Fe作负极,电极反应为Fe-2e-===Fe2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2 L的恒容密闭容器中充入A(g)和B(g),发生反应:A(g)+B(g) ![]() 2C(g)+D(s) ΔH=a kJ·mol-1实验内容和结果分别如表和图所示。下列说法正确的是( )
2C(g)+D(s) ΔH=a kJ·mol-1实验内容和结果分别如表和图所示。下列说法正确的是( )
实验 序号 | 温度 | 起始物质的量 | 热量 变化 | |
A | B | |||
Ⅰ | 600℃ | 1 mol | 3 mol | 96 kJ |
Ⅱ | 800℃ | 1.5 mol | 0.5 mol | ____ |
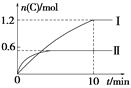
A. 实验Ⅰ中,10 min内平均速率v(B)=0.06 mol·L-1·min-1
B. 上述方程式中a=160
C. 600℃时,该反应的平衡常数是0.45
D. 向实验Ⅱ的平衡体系中再充入0.5 mol A和1.5 mol B,A的转化率增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com