
| A、加入盐酸酸化,将可能出现的沉淀过滤后,再加入Ba(NO3)2溶液 |
| B、先加入HNO3溶液酸化,再加入Ba(NO3)2溶液 |
| C、加入盐酸酸化的Ba Cl2溶液 |
| D、加入盐酸酸化,将可能出现的沉淀过滤后,再加入Ba Cl2溶液 |


 品学双优卷系列答案
品学双优卷系列答案 小学期末冲刺100分系列答案
小学期末冲刺100分系列答案 期末复习检测系列答案
期末复习检测系列答案 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案科目:高中化学 来源: 题型:
| … | E | A | B | ||
| C | … | D |
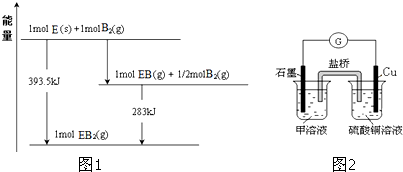
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、它们单质的熔、沸点随核电荷数的增加逐渐升高 |
| B、它们单质的颜色随核电荷数的增加逐渐加深 |
| C、它们单质的密度随核电荷数的增加逐渐增大 |
| D、它们氢化物的稳定性核电荷数的增加逐渐增强 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用蒸馏的方法制取蒸馏水 |
| B、用过滤的方法除去NaCl溶液中含有的少量淀粉胶体 |
| C、用溶解、过滤的方法提纯含有少量BaSO4的BaCO3 |
| D、粗盐提纯中用加热、蒸发的方法可以除去CaCl2、MgCl2等杂质 |
查看答案和解析>>
科目:高中化学 来源: 题型:
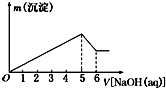 向某硫酸铝和硫酸镁的混合溶液中逐滴加入2mol?L-1的NaOH溶液,生成沉淀的质量m与加入NaOH溶液体积的关系如图所示,则原混合溶液中MgSO4与Al2(SO4)3的物质的量浓度之比为( )
向某硫酸铝和硫酸镁的混合溶液中逐滴加入2mol?L-1的NaOH溶液,生成沉淀的质量m与加入NaOH溶液体积的关系如图所示,则原混合溶液中MgSO4与Al2(SO4)3的物质的量浓度之比为( )| A、1:1 | B、1:2 |
| C、1:3 | D、2:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、5Cl2+I2+6H2O=10HCl+2HIO3 | ||||
B、2NaCl
| ||||
| C、2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O | ||||
D、2HClO
|
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com