
| A. | 熔融状态下的NaHSO4电离:NaHSO4═Na++H++SO${\;}_{4}^{2-}$ | |
| B. | Fe(OH)3的电离:Fe(OH)3?Fe3++3OH- | |
| C. | H2CO3的电离:H2CO3?2H++CO${\;}_{3}^{2-}$ | |
| D. | 水溶液中的NaHSO4电离:NaHSO4═Na++HSO${\;}_{4}^{-}$ |
分析 A.硫酸氢根离子在熔融状态下不能拆;
B.氢氧化铁为弱电解质,部分电离;
C.碳酸为多元弱酸分步电离,以第一步为主;
D.硫酸氢根离子在水溶液中完全电离.
解答 解:A.熔融状态下的NaHSO4电离,电离方程式:NaHSO4═Na++HSO42-,故A错误;
B.Fe(OH)3的电离,电离方程式:Fe(OH)3?Fe3++3OH-,故B正确;
C.H2CO3的电离,电离方程式:H2CO3?H++HCO32-,故C错误;
D.水溶液中的NaHSO4电离,电离方程式:NaHSO4═Na++H++SO42-,故D错误;
故选:B.
点评 本题考查了电解质电离方程式的书写,明确电解质强弱及电离方式是解题关键,注意弱电解质部分电离用可逆号,强电解质完全电离,用等号,注意硫酸氢根离子在熔融状态下不能拆.


科目:高中化学 来源: 题型:选择题
| A. | LiH和D2O反应,所得氢气的摩尔质量为4 g•mol-1 | |
| B. | 1 mol LiAlH4在125℃完全分解转移3 mol电子 | |
| C. | LiH与水反应的化学方程式为LiH+H2O═LiOH+H2↑ | |
| D. | LiH中微粒半径r(Li+)<r(H-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 我国历史上铅的使用早于锌 | B. | 锌和铅有相似性,但锌更活泼 | ||
| C. | 属于用热还原法冶炼金属 | D. | 所得产品中混有煤炭 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
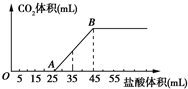
| A. | OA段发生反应的离子方程式为:H++OH-═H2O CO${\;}_{3}^{2-}$+H+═HCO${\;}_{3}^{-}$ | |
| B. | 当加入35 mL盐酸时,产生CO2的体积为224 mL | |
| C. | A点溶液中的溶质为NaCl、NaHCO3 | |
| D. | 混合物中NaOH的质量0.60 g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 非金属元素组成的化合物中只含共价键 | |
| B. | 水溶液能导电的化合物一定是离子化合物 | |
| C. | 化合物MgO、SiO2、SO3中化学键的类型相同 | |
| D. | PH3分子稳定性低于NH3分子,因为N-H键键能高 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径的大小顺序r(X)>r(Y)>r(Z)>r(R)>r(W) | |
| B. | 氢气在R的单质中燃烧火焰呈蓝色 | |
| C. | 元素X的氢化物的稳定性比Y的弱 | |
| D. | Y与Z形成的两种化合物中的化学键类型均相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2S溶液:c(Na+)>c(HS-)>c(OH-)>c(H2S) | |
| B. | Na2C2O4溶液:c(OH-)=c(H+)+c(HC2O${\;}_{4}^{-}$)+2c(H2C2O4) | |
| C. | Na2CO3溶液:c(Na+)+c(H+)=2c(CO${\;}_{3}^{2-}$)+c(OH-) | |
| D. | CH3COONa溶液:c(Na+)>c(CH3COO-) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| Fe3+ | Co2+ | Co3+ | Al3+ | |
| pH(开始沉淀) | 1.9 | 7.15 | -0.23 | 3.4 |
| pH(完全沉淀) | 3.2 | 9.15 | 1.09 | 4.7 |
| 温度范围/℃ | 固体质量/g |
| 150~210 | 4.41 |
| 290~320 | 2.41 |
| 890~920 | 2.25 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 通入HCl | B. | 加少量NH4Cl固体 | C. | 加少量NaCl固体 | D. | 通入氨气 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com