
【题目】如图是部分短周期元素的单质及其化合物(或溶液)的转化关系,已知单质 B2、C2、D2、E2 在常温常压下都是气体,化合物 G 在焰色反应中显黄色;化合物I、J、K 通常状况下呈气态。下列说法正确的是
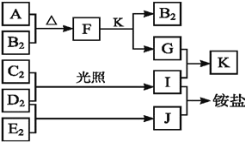
A.E 的氢化物沸点高于B 的氢化物沸点
B.G 为强碱弱酸盐,可用于厨房去油污
C.F 中既含有离子键又含有极性共价键
D.原子半径:A>C>B>E>D
【答案】B
【解析】
I与J反应生成铵盐,则它们分别是NH3与HX(X代表卤素,短周期中是F、Cl中的一种,下同),得到这两种氢化物的反应物是N2、H2、X2,共同需要的反应物D2为H2,从反应条件看,H2与X2可以光照生成HX,而N2与H2反应生成NH3需要在催化剂加热加压条件下才能合成,所以C2为Cl2,E2为N2,I为HX,J为NH3。G的焰色反应为黄色,说明G是钠的化合物,反应生成气体K,则可能G是钠的碳酸盐(包括酸式盐)反应生成CO2,或G是钠的亚硫酸盐(包括酸式盐)反应生成SO2,则F是钠的另一种化合物且能够与CO2(或SO2)反应生成相应的上述盐类,同理,A或B中含有钠元素,由于B2是气体,则A中含有钠元素。结合已学反应原理,A是Na单质,B2是O2,二者加热生成Na2O2,K只能是CO2,G是Na2CO3,因为Na2O2与SO2反应生成Na2SO4,不能再与HCl反应生成SO2。
A.E的氢化物为NH3,B的氢化物为H2O,H2O的沸点高于NH3的沸点,A错误;
B.G为碳酸钠,为强碱弱酸盐,可以用于厨房去油,B正确;
C.F为Na2O2,含有离子键和非极性共价键,C错误;
D.A到E五种元素依次为Na、O、Cl、H、N,半径顺序为Na>Cl>N>O>H,与选项不符,D错误;
故选B。


科目:高中化学 来源: 题型:
【题目】根据要求回答问题:
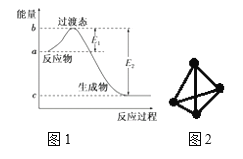
(1)图1是1 mol NO2(g)和1 mol CO(g)反应生成CO2和NO过程中的能量变化示意图,若在反应体系中加入催化剂,反应速率增大,E1的变化是________(填“增大”、“减小”或“不变”,下同),ΔH的变化是________。
(2)已知CH3OH(l)的燃烧热为726.5kJ·mol-1,CH3OH(l)+ 1/2O2(g)═CO2(g)+2H2(g)△H= -a kJ·mol-1 ,则a________726.5(填“>”、“<”或“=”)。
(3)科学家已获得了极具理论研究意义的N4分子,其结构为正四面体(如图2所示),与白磷分子相似。已知断裂1mol N-N键吸收193 kJ热量,断裂1 mol N≡N键吸收941 kJ热量,则1 mol N4气体转化为2 mol N2时的△H= ________。
(4)在微生物作用的条件下,NH4+经过两步反应被氧化成NO3-。这两步的能量变化如图:
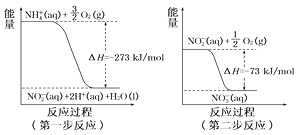
第二步反应是________反应(填“放热”或“吸热”)。1 mol NH4+(aq)全部氧化成NO3-(aq)的热化学方程式是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳呼吸电池被誉为改变世界的创新技术,设想用碳呼吸电池为锂硫电池充电的装置如下图所示,下列说法不正确的是
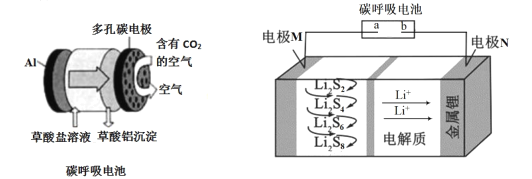
A.a极是多孔碳电极
B.充电时,外电路中流过0.02 mol电子,电极N质量增加0.14 g
C.随着反应的进行,碳呼吸电池中C2O42- 数目不断减小
D.充电时间越长,电池中的Li2S8量越多
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮化锶(Sr3N2)在工业上广泛用于生产荧光粉。锶与氮气在加热条件下可生成氮化锶,氮化锶遇水剧烈反应。某同学设计如下装置制备氮化锶(各装置盛装足量试剂),所使用的氮气样品可能含有少量CO、CO2、O2等气体杂质。
已知:醋酸二氨合亚铜CH3COO[Cu(NH3)2]溶液能定量吸收CO,但易被O2氧化,失去吸收CO能力;连苯三酚碱性溶液能定量吸收O2。
Ⅰ.氮化锶的制取
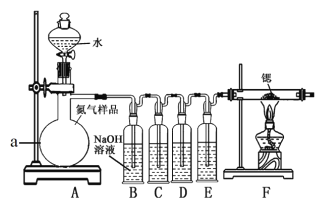
(1)仪器a的名称是__________________。
(2)装置C、D、E盛装的试剂分别是_______________(填代号)。
甲. 连苯三酚碱性溶液
乙. 浓硫酸
丙. 醋酸二氨合亚铜溶液
(3)该套装置设计存在缺陷,可能会导致产品变质,提出改进方案 ____。
Ⅱ.产品纯度的测定
称取6.0 g Ⅰ中所得产品,加入干燥的三颈烧瓶中,然后由恒压滴液漏斗加入蒸馏水,通入水蒸气,将产生的氨全部蒸出,用200.00 mL 1.00 mol/L的盐酸标准溶液完全吸收(吸收液体积变化忽略不计)。从烧杯中量取20.00 mL的吸收液,用1.00 mol/L NaOH标准溶液滴定过剩的HCl,到终点时消耗16.00 mL NaOH溶液。(图中夹持装置略)
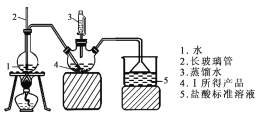
(4)三颈烧瓶中发生反应的化学方程式为 _________________________________。
(5)装置中长玻璃管的作用原理是_________。
(6)用1.00 mol/L的NaOH标准溶液滴定过剩的 HCl时所选指示剂为__________________。
(7)产品纯度为_____________。(保留三位有效数字)
(8)下列实验操作可能使氮化锶(Sr3N2)测定结果偏低的是____________(填字母)。
a.滴定前碱式滴定管未排气泡,滴定后气泡消失
b. 读数时,滴定前平视,滴定后俯视
c. 滴定后,碱式滴定管尖嘴外还悬着一滴液体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】KIO3 是一种重要的无机化合物,常作为食盐中的补碘剂,工业上常用“KClO3 氧化法”制备 KIO3,其中酸化反应的产物有 KH(IO3)2、Cl2 和 KCl,流程如下:
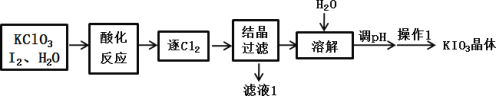
下列说法错误的是
A.酸化反应中还原产物为 KH(IO3)2
B.结晶过滤得到滤液 1 为 KCl 溶液
C.调节 pH 可加入 KOH,发生反应 KH(IO3)2+ KOH=2KIO3+ H2O
D.操作 1 可采用蒸发浓缩、冷却结晶的方法
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是硫酸试剂瓶标签上的内容:

![]() 该硫酸的物质的量浓度为______
该硫酸的物质的量浓度为______![]() 。
。
![]() 某化学小组进行硫酸酸性实验探究时,需要配制
某化学小组进行硫酸酸性实验探究时,需要配制![]() 的稀硫酸,则需要取上述的浓硫酸______mL。
的稀硫酸,则需要取上述的浓硫酸______mL。
(3)下列情况使所配制硫酸溶液物质的量浓度偏高的是________,
A.未经冷却趁热将溶液注入容量瓶中
B.定容时仰视读数
C.移液时不慎将少量溶液滴在容量瓶外面
D.用量筒量取浓硫酸时仰视读数
E.加蒸馏水时不慎超过了刻度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分下图中X是无支链的、具有果香味的合成香料,可用于调配多种果香型香精。已知
D在标准状况下的密度为1.25 g/L,其产量可以用来衡量一个国家石油化工发展水平。E是生活
中常见的一种有机物。各物质间转化关系如下:
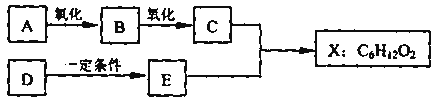
请回答下列问题。
(1)A的名称是________________________。
(2)B中所含的官能团是________________。
(3)C+E![]() X的化学反应类型是___________________反应。
X的化学反应类型是___________________反应。
(4)写出任意两种与A具有相同官能团的A的同分异构体的结构简式 (不含A):_________。
(5)X与氢氧化钠溶液反应的化学方程式是______________________________。
(6)以D为原料生产一种常见塑料的化学方程式是___________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】卤素互化物与卤素单质性质相似。已知CH2=CH—CH=CH2(1,3—丁二烯)与氯气发生1:1加成的产物有两种:
①CH2Cl—CHCl—CH=CH2(1,2—加成) ②CH2Cl—CH=CH—CH2Cl (1,4—加成)
据此推测CH2=C(CH3)—CH=CH2(异戊二烯)与卤素互化物BrCl的1:1加成产物有几种(不考虑顺反异构和镜像异构( )
A. 6种B. 10种C. 12种D. 14种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在T ℃时,难溶物Ag2CrO4在水溶液中的溶解平衡曲线如下图所示,又知T ℃时AgCl的Ksp=1.8×10-10。下列说法错误的是

A. T ℃时,Ag2CrO4的Ksp为1×10-11
B. T ℃时,Y点和Z点的Ag2CrO4的Ksp相等
C. T ℃时 , X点的溶液不稳定,会自发转变到Z点
D. T ℃时,将0.01 mol·L-1的AgNO3溶液逐渐滴入20 mL 0.01 mol·L-1的KCl和0.01 mol·L-1的K2CrO4混合溶液中,Cl-先沉淀
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com