
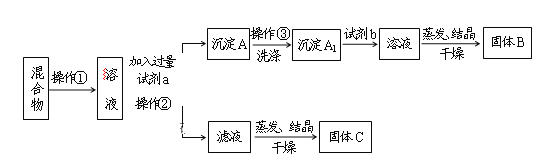
【题目】某同学设计如下实验方案,以分离KCl和BaCl2两种固体混合物,试回答下列问题:
供选试剂:Na2SO4溶液、K2SO4溶液、K2CO3溶液、盐酸
(1)操作①的名称是___,操作②的名称是___。
(2)试剂a是___,固体B是___。(填化学式)
(3)生成沉淀A的离子反应方程式为:__加入试剂b所发生的化学反应方程式为:___。
(4)该方案能否达到实验目的:___。若不能,应如何改进(若能,此问不用回答)___。
(5)若要测定原混合物中KCl和BaCl2的质量分数,除了要准确称量混合物的质量外,至少还要获得的数据是____的质量。
【答案】溶解 过滤 K2CO3 BaCl2 CO32-+Ba2+=BaCO3↓ BaCO3+2HCl=BaCl2+H2O+CO2↑ 不能 滤液中有过量的CO32-未除去,应加入稀盐酸除去 BaCl2(或:固体B或沉淀A1的质量)
【解析】
分离KCl和BaCl2两种固体混合物,可先溶于水,然后加入过量K2CO3使BaCl2转化为沉淀,过滤后沉淀加入盐酸可生成BaCl2溶液,经蒸发、结晶、干燥后可得固体BaCl2,操作②所得滤液为KCl和K2CO3的混合物,应加入过量盐酸可得KCl。
(1)将固体配成溶液,应加水溶解,操作②为固体和液体的分离,为过滤操作;
(2)固体溶解后加入过量K2CO3使BaCl2转化为沉淀,过滤后沉淀加入盐酸可生成BaCl2溶液,经蒸发、结晶、干燥后可得固体BaCl2;
(3)加入试剂a,K2CO3与BaCl2反应生成BaCO3沉淀,发生的离子方程式为CO32-+Ba2+=BaCO3↓,加入试剂b,BaCO3沉淀加入盐酸可生成BaCl2溶液,反应的化学方程式为:BaCO3+2HCl=BaCl2+H2O+CO2↑。
(4)滤液为KCl和K2CO3的混合物,⑥蒸发结晶前应加入适量稀盐酸,将过量的碳酸钾转化成氯化钾。
(5)固体溶解后加入过量K2CO3使BaCl2转化为碳酸钡沉淀,过滤后沉淀加入试剂b盐酸可将碳酸钡转化成BaCl2溶液,然后经蒸发、结晶、干燥后可得固体BaCl2,若要测定原混合物中KCl和BaCl2的质量分数,除了要准确称量混合物的质量外,至少还要获得的数据是固体B或沉淀A1的质量,依据B为BaCl2计算得到质量分数,A1为碳酸钡,结合钡元素守恒计算氯化钡质量得到,故少还要获得的数据是:固体B或沉淀A1的质量。


 全优考典单元检测卷及归类总复习系列答案
全优考典单元检测卷及归类总复习系列答案科目:高中化学 来源: 题型:
【题目】400 ℃时,将一定量的SO2和 14 mol O2压入一个盛有催化剂的10 L密闭容器中进行反应:2SO2+O2 ![]() 2SO3
2SO3
已知 2 min后,容器中剩余 2 mol SO2和12 mol O2。试计算:
(1)生成SO3的物质的量。______
(2)SO2的起始物质的量浓度。______
(3)2 min 内SO2和SO3的反应速率。______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】T℃时,水的离子积为Kw,该温度下将a mol/L一元酸HA溶液与b mol/L一元碱BOH溶液等体积混合,若混合后溶液呈中性,则下列说法一定正确的是( )
A. 混合液中,c(H+) = ![]() B. 混合液的pH=7
B. 混合液的pH=7
C. 混合液中,c(B+) = c(A-) + c(OH-) D. a = b
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】发展新能源汽车是国家战略,经过近10年的发展,目前我国新能源汽车产销量均达到80万辆,LiFePO4电池是新能源汽车关键部件之一,其工作原理如图所示。下列说法错误的是( )
A. 充电时,电极a与电源的负极连接,电极b与电源正极连接
B. 电池驱动汽车前进时,正极的电极反应为:Li1-xFePO4+x Li++x e-= LiFePO4
C. 电池驱动汽车后退时,负极材料减重1.4g ,转移0.4mol电子
D. 电池进水将会大大降低其使用寿命
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】重铬酸钠是一种用途极广的氧化剂,工业上可以用铬铁矿[主要成分Fe(CrO2)2(或写成FeO·Cr2O3),还含有Al2O3、Fe2O3、SiO2等杂质]制备,同时还可回收Cr。其主要工业流程如图所示:

已知部分物质的溶解度曲线如图1所示。


图1 图2
请回答下列问题:
(1)煅烧生成Na2CrO4的化学方程式为______________________________。
(2)煅烧后的浸出液中除了含有NaOH、Na2CO3、Na2CrO4外,还含有_________(填化学式)。
(3)调节溶液的pH所选的试剂为__________________(填名称)。
(4)操作a的实验步骤为 _________________________。
(5)加入Na2S溶液反应后,硫元素全部以S2O32-的形式存在,写出生成Cr(OH)3的离子方程式__________________________________。
(6)采用石墨电极电解Na2CrO4溶液制备Na2Cr2O7,其原理如图2所示。
①写出电极b的电极反应方程式:___________________________________。
②测定阳极液中Na元素和Cr元素的含量,若Na元素与Cr元素的物质的量之比为n,则此时Na2CrO4的转化率为____________。
(7)根据有关国家标准,含CrO42-的废水要经化学处理,使其浓度降至5.0×10-7mol·L-1 以下才能排放。可采用加入可溶性钡盐生成BaCrO4沉淀[Ksp(BaCrO4)=1.2×10-10],再加入硫酸处理多余的Ba2+的方法处理废水,加入可溶性钡盐后,废水中Ba2+的浓度应不小于___________mol·L-1 ,废水处理后方能达到国家排放标准。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮(N)、磷(P)、砷(As)等VA族元素的化合物在研究和生产中有重要用途,请回答下列问题:
(1)基态磷原子的电子排布图为________________,与砷原子同周期且含有的未成对电子数相同的元素有________种。
(2)(SCN)2分子中各元素的电负性由大到小的顺序为______________(用元素符号表述),分子中σ键和п键个数比为____________,(SCN)2能与Cu2+形成配合物,理由是_______________________________。
(3)CO2是N2O的等电子体,N2O中中心原子的杂化轨道类型为_______________。
(4)砷的一种氧化物俗称“砒霜”,我国科研人员研究发现砒霜对白血病有明显的治疗作用,其结构如图1所示,“砒霜”的化学式为___________,“砒霜”在一定条件下能转化成Na3AsO4,Na3AsO4中阴离子的空间构型为____________________。


图1 图2
(5)磷化硼是一种耐磨材料,其晶胞结构如图2所示,晶体中一个B原子周围距离最近的P原子有____个;若B、P原子半径分别为r1pm和r2pm,阿伏加德罗常数值为NA,晶体密度为d g/cm3,则磷化硼晶胞中原子的体积占晶胞体积的百分率为________ ×100% (用含d、r1、r2 的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成乙烯的主要反应:6H2(g)+2CO2(g)![]() CH2=CH2(g)+4H2O(g) △H<0。图中L(L1、L2)、Ⅹ可分别代表压强或温度。下列说法正确的是
CH2=CH2(g)+4H2O(g) △H<0。图中L(L1、L2)、Ⅹ可分别代表压强或温度。下列说法正确的是
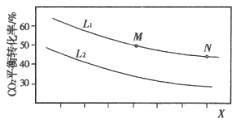
A. L1<L2
B. X代表压强
C. M、N两点对应的平衡常数相同
D. M点的正反应速率v正小于N点的逆反应速率v逆
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 将饱和FeCl3溶液滴入沸水中制胶体,离子方程式:Fe3++3H2O![]() Fe(OH)3 ↓+3H+
Fe(OH)3 ↓+3H+
B. 为确定某酸H2A是强酸还是弱酸,可测NaHA溶液的pH。若pH>7,则H2A是弱酸;若pH<7,则H2A是强酸
C. 一定条件下使化学平衡向正反应方向移动,反应物的转化率不一定增大
D. 升温时,若某可逆反应化学平衡常数K值变小,则表明该反应的ΔH>0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化硫是大气的主要污染物之一。催化还原SO2不仅可以消除SO2的污染,还可以得到工业原料S。燃煤烟气中硫的回收反应为:2CO(g)+SO2(g) ![]() 2CO2(g)+S(l) △H。
2CO2(g)+S(l) △H。
(1)已知:2CO(g)+O2(g)===2CO2(g) △H1=-566.0kJ·mol-1
S(l)+O2(g)===SO2(g) △H2=-296.8 kJ·mol-1
则硫的回收反应的△H=___________ kJ·mol-1。
(2)其他条件相同、催化剂不同时,硫的回收反应中SO2的转化率随反应温度的变化如图所示。260℃时,___________(填“La2O3”、“NiO”或“TiO2”)的催化效率最高。La2O3和NiO作催化剂均可能使SO2的转化率达到很高,不考虑价格因素,选择La2O3的主要优点是___________。

(3)一定条件下,若在恒压密闭容器中发生硫的回收反应,SO2的平衡转化率与温度、压强的关系如图所示,则P1、P2、P3、P4由大到小的顺序为___________;某温度下,若在恒容密闭容器中,初始时c(CO)=2 a mol·L-1,c(SO2)= a mol·L-1,SO2的平衡转化率为80%,则该温度下反应的化学平衡常数为___________。
(4)某实验小组为探究烟气流速、温度对该反应的影响,用La2O3作催化剂,分别在两种不同烟气流量、不同温度下进行实验。实验结果显示:在260℃时,SO2的转化率随烟气流量增大而减小,其原因是___________;在380℃时,SO2的转化率随烟气流量增大而增大,其原因是___________。
(5)工业上常用Na2SO3溶液吸收烟气中的SO2,将烟气通入1.0 mol·L-1的N2SO3溶液,当溶液pH约为6时,吸收SO2的能力显著下降此时溶液中c(HSO3-)c︰(SO32-)=___________。(已知H2SO3的Ka1=1.5×10-2、Ka2=1.0×10-7)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com