
【题目】向80mL 0.1molL-1稀HNO3溶液中加入铜粉和铁粉混合物,固体完全溶解,在反应后溶液中滴加硫氰化钾溶液,溶液没有出现血红色。铜粉和铁粉混合物的质量可能是
A.0.168gB.0.184gC.0.192gD.0.200g
【答案】B
【解析】
稀HNO3溶液中加入铜粉和铁粉混合物,固体完全溶解,在反应后溶液中滴加硫氰化钾溶液,溶液没有出现血红色,则反应生成Cu(NO3)2、Fe(NO3)3,由于硝酸可以氧化亚铁离子,故硝酸没有剩余,n(HNO3) = 0.08L![]() 0.1mol/L = 0.008mol,由3A + 8HNO3 = 3A(NO3)3+ 2NO↑+4H2O,则n(Cu) + n(Fe) = 0.008mol
0.1mol/L = 0.008mol,由3A + 8HNO3 = 3A(NO3)3+ 2NO↑+4H2O,则n(Cu) + n(Fe) = 0.008mol![]() = 0.003mol,全部为Cu时,金属质量最大,最大质量为0.003mol
= 0.003mol,全部为Cu时,金属质量最大,最大质量为0.003mol![]() 64g/ mol = 0.192g;全部为Fe时,计算质量最小,最小质量为0.003mol
64g/ mol = 0.192g;全部为Fe时,计算质量最小,最小质量为0.003mol ![]() 56g/ mol = 0.168g,故混合物质量介于0.168g~0.192g之间,所以B符合题意;
56g/ mol = 0.168g,故混合物质量介于0.168g~0.192g之间,所以B符合题意;
故答案:B。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】“立方烷”是新合成的一种烃,其分子为正立方体结构。
(1)“立方烷”的分子式是_____。
(2) “立方烷”分子中可能有的结构是_____。(从A、B、C、D中选)。
A.![]()
B.![]()
C.
D.![]()
(3) “立方烷”可能发生的反应或变化有_____。(从A、B、C、D中选)。
A.可使Br2水褪色,但不反应
B.不能使溴的CCl4溶液褪色
C.能发生取代反应
D.能发生加成反应
(4) “立方烷”的一种同分异构体为芳香烃,此芳香烃能发生加聚反应,其结构简式为_____,发生的加聚反应化学方程式为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业废弃物的资源化回收再利用,可以更大限度地发挥原材料的价值。某教师在指导学生做研究性学习时,拟利用废铁屑在实验室制备FeSO4溶液,再与等物质的量的(NH4)2SO4反应,制备补血剂硫酸亚铁铵晶体[(NH4)2Fe(SO4)2·6H2O,相对分子质量为392]。硫酸亚铁铵晶体比一般亚铁盐稳定,在空气中不易被氧化,易溶于水,不溶于乙醇。
(1)废铁屑的净化:将废铁屑投入10%的碳酸钠溶液中并加热5~10min,通过倾析法弃去纯碱溶液,并用蒸馏水洗净废铁屑,待用。
(2)酸浸净化后的废铁屑:将2gFe粉、10mL3mol·L-1的H2SO4溶液加入烧瓶中反应,用如图所示装置制备FeSO4溶液。保持温度70~80℃,适当添加水以补充被蒸发掉的水分,并控制溶液的pH,至反应无明显气泡产生,停止加热,过滤,称量残留固体质量。
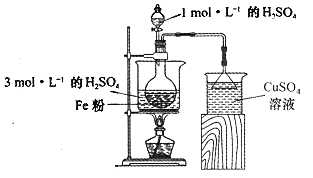
①反应过程中会产生少量H2S、PH3等气体,需使用封闭装置。写出用CuSO4溶液吸收H2S气体的化学反应方程式:____________________________
②反应过程中使用过量铁粉的目的是____________________________
(3)制备(NH4)2Fe(SO4)2·6H2O:向FeSO4溶液中加入一定质量的(NH4)2SO4固体,70~80℃条件下溶解后,趁热倒入50mL乙醇中,析出晶体。
实验中,需对过滤出产品的母液(pH<1)进行处理。室温下,分别取母液并向其中加入指定物质,反应后的溶液中主要存在的一组离子正确的是_____ (填序号)。
A.通入过量Cl2:Fe2+、H+、NH4+、Clˉ、SO42ˉ
B.加入过量KSCN溶液:K+、NH4+、Fe3+、SO42ˉ、SCNˉ
C.加入过量NaOH溶液:Na+、Fe2+、NH4+、SO42ˉ、OHˉ
D.加入过量NaClO和NaOH的混合溶液:Na+、SO42ˉ、Clˉ、ClOˉ、OHˉ
(4)产品纯度测定:称取ag产品溶于水,配制成500mL溶液,取25.00mL待测液,用浓度为cmol·L-1的酸性KMnO4溶液滴定。重复上述操作2次实验结果如下:

该产品的纯度为____________________________(用含a、c的代数式表示)。
有同学提出,测定产品中SO42ˉ的含量也可测定产品的纯度,请补充完整实验方案:称取约0.4g样品,溶于70mL水,__________________________________________________,将沉淀移入坩埚,灼烧至恒重,记录数据(实验中必须使用的试剂有:2mol·L-1的HCl溶液、BaCl2溶液、AgNO3溶液)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,在容积为1L的密闭容器中充入![]() 和
和![]() 发生
发生![]() 测得
测得![]() 的物质的量随时间的变化如图所示,(已知,此温度下,该反应的平衡常数
的物质的量随时间的变化如图所示,(已知,此温度下,该反应的平衡常数![]() )下列说法正确的是 ( )
)下列说法正确的是 ( )
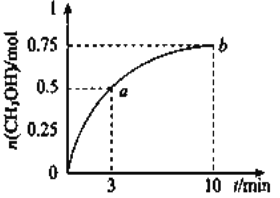
A. ![]()
B. 点b所对应的状态为化学平衡状态
C. ![]() 的生成速率,点a低于点b
的生成速率,点a低于点b
D. 欲增大平衡状态时![]() ,可保持其他条件不变,升高温度
,可保持其他条件不变,升高温度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学式为C2H6O的化合物A具有如下性质:A+Na―→慢慢产生气泡
A+CH3COOH![]() 有香味的产物
有香味的产物
(1)根据上述信息,对该化合物可作出的判断是(____)。
A.一定含有—OH B.一定含有—COOH
C.A为乙醇 D.A为乙醛
(2)含A的体积分数为75%的水溶液可以用作______。
(3)A与钠反应的化学方程式:_____________。
(4)化合物A与CH3COOH反应生成的有香味的产物的结构简式为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列溶液中一定大量共存的离子组是( )
A.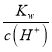 =0.1 mol L1 的溶液:Na+、K+、CO32-、NO3-
=0.1 mol L1 的溶液:Na+、K+、CO32-、NO3-
B.含有大量 S2-的溶液中:K+、Fe3+、ClO-、SO42-
C.能使 Al3+生成沉淀的溶液中:NH4+、Na+、SiO32-、HCO3-
D.水电离产生的 c(OH-)=1×10-10 mol/L 的溶液中:Fe2+、SO42-、NO3-、Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高纯硫酸锰作为合成镍钴锰三元正极材料的原料,工业上可由天然二氧化锰粉与硫化锰矿(还含Fe、Al、Mg、Zn、Ni、Si等元素)制备,工艺如下图所示。回答下列问题:
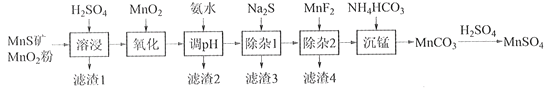
相关金属离子[c0(Mn+)=0.1 mol·L1]形成氢氧化物沉淀的pH范围如下:
金属离子 | Mn2+ | Fe2+ | Fe3+ | Al3+ | Mg2+ | Zn2+ | Ni2+ |
开始沉淀的pH | 8.1 | 6.3 | 1.5 | 3.4 | 8.9 | 6.2 | 6.9 |
沉淀完全的pH | 10.1 | 8.3 | 2.8 | 4.7 | 10.9 | 8.2 | 8.9 |
(1)“滤渣1”含有S和__________________________;写出“溶浸”中二氧化锰与硫化锰反应的化学方程式____________________________________________________。
(2)“氧化”中添加适量的MnO2的作用是将________________________。
(3)“调pH”除铁和铝,溶液的pH范围应调节为_______~6之间。
(4)“除杂1”的目的是除去Zn2+和Ni2+,“滤渣3”的主要成分是______________。
(5)“除杂2”的目的是生成MgF2沉淀除去Mg2+。若溶液酸度过高,Mg2+沉淀不完全,原因是_____________________________________________________________________。
(6)写出“沉锰”的离子方程式___________________________________________________。
(7)层状镍钴锰三元材料可作为锂离子电池正极材料,其化学式为LiNixCoyMnz2,其中Ni、Co、Mn的化合价分别为+2、+3、+4。当x=y=![]() 时,z=___________。
时,z=___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为提升电池循环效率和稳定性,科学家近期利用三维多孔海绵状Zn(3DZn)可以高效沉积ZnO的特点,设计了采用强碱性电解质的3DZn—NiOOH二次电池,结构如下图所示。电池反应为Zn(s)+2NiOOH(s)+H2O(l)![]() ZnO(s)+2Ni(OH)2(s)。
ZnO(s)+2Ni(OH)2(s)。

A. 三维多孔海绵状Zn具有较高的表面积,所沉积的ZnO分散度高
B. 充电时阳极反应为Ni(OH)2(s)+OH(aq)e![]() NiOOH(s)+H2O(l)
NiOOH(s)+H2O(l)
C. 放电时负极反应为Zn(s)+2OH(aq)2e![]() ZnO(s)+H2O(l)
ZnO(s)+H2O(l)
D. 放电过程中OH通过隔膜从负极区移向正极区
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com