
煤的气化所得气体可用于城市家用燃气。下列选项中的气体均属于家用燃气有效成分的是
A.CO、H2、N2 B.CO、CH4、H2 C.CO、CH4、CO2 D.CH4、H2、O2
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
在C(s)+CO2(g)===2CO(g)的反应中,现采取下列措施:
①缩小体积,增大压强 ②增加碳的量 ③通入CO2 ④恒容下充入N2
⑤恒压下充入N2能够使反应速率增大的措施是( )
A.①④ B.②③⑤ C.①③ D.①②④
查看答案和解析>>
科目:高中化学 来源: 题型:
某芳香族化合物A式量小于150,氢氧质量比为1∶8,完全燃烧后只生成CO2和H2O。取等质量的A分别与足量NaHCO3和Na反应,生成的气体在同温同压下的体积比为1∶1。工业常用A来合成药物B及医药中间体G,流程如下:

已知:
|
|
(1)写出A含有的官能团的名称 ,D的结构简式 。
(2)D生成E的反应类型是 。
(3)A合成B的同时,A自身之间也能发生缩聚反应,写出该缩聚反应的化学方程式
。
(4)写出F与过量NaOH共热时反应的化学方程式 。
(5)B有多种同分异构体,写出符合下列条件的一种物质的结构简式 。
①只有一种官能团
②能发生银镜反应
③苯环上的一氯取代物只有二种
④核磁共振谱共有四组峰,个数比为3∶2∶2∶1。
(6)下列有关说法正确的是 。
A.可由A经一步反应获得D
| B. |
| 与G互为同分异构体 |
C.G易水解,可用FeCl3溶液检验是否发生水解
D.1molG一定能和5mol氢气反应
查看答案和解析>>
科目:高中化学 来源: 题型:
将0.2 mol丁烷完全燃烧后生成的气体全部缓慢通入0.5 L 2 mol/L NaOH溶液中,生成的Na2CO3和NaHCO3的物质的量之比为( )
A.3∶2 B.2∶3 C.2∶1 D.1∶3
查看答案和解析>>
科目:高中化学 来源: 题型:
M元素的1个原子失去2个电子转移到Y元素的2个原子中去,形成离子化合物Z。下列说法中正确的是( )
A. Z可表示为MY2
B. Z可表示为M2Y
C. Z的电子式可表示为

D. M形成+2价阳离子
查看答案和解析>>
科目:高中化学 来源: 题型:
甲、乙两同学欲验证乙醇的性质,现做如下实验:
Ⅰ.甲同学做乙醇的催化氧化实验并考查催化剂的催化机理,现设计了如图装置(夹持装置仪器已省略),

其实验操作为:先按图安装好,关闭活塞a、b、c,在铜丝的中间部分加热片刻,然后打开活塞a、b、c,通过控制活塞a和b,而有节奏(间歇性)地通入气体,即可在M处观察到明显的实验现象。试回答以下问题:
(1)A中发生反应的化学方程式:_____________________________________________________ ,
B的作用:________________________ ;C中热水的作用:___________________________ 。
(2)M处发生反应的化学方程式为:_____________________________________________________ 。
(3)从M管中可观察到的现象:________________________________________________________ 。
 从中可认识到该实验过程中催化剂________(填“参加”或“不参加”)了化学反应,还可以认识到催化剂起催化作用需要一定的_________________ 。
从中可认识到该实验过程中催化剂________(填“参加”或“不参加”)了化学反应,还可以认识到催化剂起催化作用需要一定的_________________ 。
Ⅱ.乙同学进行乙醇的沸点测定实验,设计装置如图,回答下列问题:
(1)盛乙醇的试管应浸入水浴中,水浴的温度应保持在___________ 。
A.100 ℃ B.78.5 ℃ C.80 ℃ D.50 ℃
(2)测乙醇沸点时为什么不把整个试管浸在水里?______________________;
为什么塞子上要有个豁口?_____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
在2A+B 3C+5D反应中,表示该反应的速率最快的是
3C+5D反应中,表示该反应的速率最快的是
A.υ(A)= 30 mol/(L ·min) B.υ(B)= 0.3 mol/(L ·s)
C.υ(C)= 0.8 mol/(L ·s) D.υ(D)= 1 mol/(L ·s)
查看答案和解析>>
科目:高中化学 来源: 题型:
新型净水剂高铁酸钾(K2FeO4 )为暗紫色固体,可溶于水,在中性或酸性溶液中逐渐分解,在碱性溶液中稳定。
)为暗紫色固体,可溶于水,在中性或酸性溶液中逐渐分解,在碱性溶液中稳定。
工业上制备K2FeO4的常用方法有两种。
方法Ⅰ:次氯酸盐氧化法。
工艺流程如图所示。
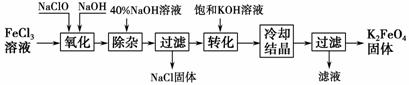
( 1)完成“氧化”过程中反应的化学方程式:
1)完成“氧化”过程中反应的化学方程式: 
 ________FeCl3+________NaOH+________NaClO→________Na2FeO4+________ +________ 。其中氧化剂是________(填化学式)。
________FeCl3+________NaOH+________NaClO→________Na2FeO4+________ +________ 。其中氧化剂是________(填化学式)。
(2)“转化”过程中发生反应的化学方程式为____________________________
______________________________________________________________。
(3)上述工艺得到 的高铁酸钾常含有杂质,可用重结晶法提纯,操作是:将粗产品用________________溶解,然后________________
的高铁酸钾常含有杂质,可用重结晶法提纯,操作是:将粗产品用________________溶解,然后________________
方法Ⅱ:电解法。
以铁为阳极电解氢氧化钠溶液,然后在阳极液中加入KOH。
(4)电解时阳极发生反应生成FeO42-, 该电极反应方程式为________________________________________________________________。
该电极反应方程式为________________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com