
| A. | 往某固体中滴加稀盐酸有气泡产生--该固体一定是碳酸盐 | |
| B. | 往某溶液中滴加氯化钡溶液,产生不溶于稀硝酸的白色沉淀--该溶液一定含有硫酸根离子 | |
| C. | 生石灰块投入水中,水会沸腾--生石灰变成熟石灰的过程是放热反应 | |
| D. | 往品红溶液中通入某种气体,使品红褪色--该气体一定是二氧化硫 |
分析 A.能和稀盐酸反应生成气体的物质可能是金属、过氧化钠、碳酸盐、碳酸氢盐、亚硫酸盐、亚硫酸氢盐等;
B.能和氯化钡溶液反应生成不溶于稀硝酸的离子有阴离子、硫酸根离子等;
C.反应物总能量小于生成物总能量,则该反应是放热反应;
D.能使品红溶液褪色的气体不一定是二氧化硫.
解答 解:A.能和稀盐酸反应生成气体的物质可能是金属、过氧化钠、碳酸盐、碳酸氢盐、亚硫酸盐、亚硫酸氢盐等,所以该固体不一定是碳酸盐,故A错误;
B.能和氯化钡溶液反应生成不溶于稀硝酸的离子有阴离子、硫酸根离子等,所以该溶液中不一定含有硫酸根离子,故B错误;
C.反应物总能量小于生成物总能量,则该反应是放热反应,生石灰块投入水中,水会沸腾,说明温度升高,反应物总能量小于生成物总能量,则该反应是放热反应,故C正确;
D.能使品红溶液褪色的气体不一定是二氧化硫,如氯气、臭氧等都能使品红溶液褪色,故D错误;
故选C.
点评 本题考查化学实验方案评价,为高频考点,明确物质的性质是解本题关键,侧重考查学生发散思维能力,熟悉常见物质的性质即可解答,易错选项是D.


 智能训练练测考系列答案
智能训练练测考系列答案科目:高中化学 来源: 题型:选择题
| X | Y | ||
| Z | W | R |
| A. | 原子半径的大小顺序:Z>X>Y | |
| B. | W、Y的气态氢化物的稳定性:W>Y | |
| C. | Z单质一定是金属铝 | |
| D. | W、R的最高价氧化物对应水化物的酸性:W>R |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K+、Cu2+、Cl-、AlO2- | B. | Na+、Al3+、NO3-、HCO3- | ||
| C. | Na+、H+、NO3-、SO42- | D. | Ca2+、Cl-、CO32-、NH4+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 混合物里三种物质反应时消耗盐酸的物质的量之比为1:1:3 | |
| B. | 反应后所得溶液中的Fe2+离子与Cl-离子的物质的量之比为1:2 | |
| C. | 混合物里,FeO的物质的量无法确定,但Fe和Fe2O3的物质的量一样多 | |
| D. | 混合物里,Fe2O3的物质的量无法确定,但Fe比FeO的物质的量多 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
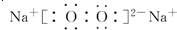 .
.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 用CO表示反应速率 | B. | 平衡混合气体的平均相对分子质量 | ||
| C. | CO的转化率 | D. | CO2的体积分数 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HCO3-、Na+、H+ | B. | Cu2+、HCO3-、OH- | C. | OH-、A13+、SO42- | D. | Mg2+、Ca2+、NO3- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com