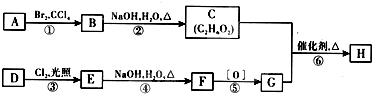
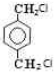
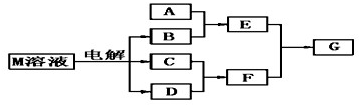
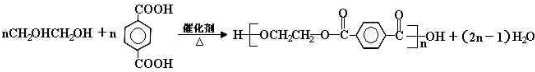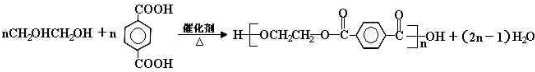(2011?许昌模拟)已知物质M由属于同一周期的X.Y两种短周期元素组成,X原子的最外层电子数是最内层电子数的一半,Y元素最高正价与它的负价代数和为6.M与其他物质的转化关系如下(部分产物已略去):
(1)已知元素Z与Y是最外层电子数相同的短周期元素,那么Z与Y分别与氢形成的氢化物中沸点较高的是
HF
HF
(填化学式),原因是
F元素电负性很强,HF分子之间可以形成氢键
F元素电负性很强,HF分子之间可以形成氢键
;
(2)若A是一种常见的酸性氧化物,且可用于制造玻璃,则E溶液与F溶液反应的离子方程式是:
SiO32-+2H++2H2O=H4SiO4↓或SiO32-+2H+=H2SiO3↓
SiO32-+2H++2H2O=H4SiO4↓或SiO32-+2H+=H2SiO3↓
;
(3)若A是与X、Y同周期元素的一种常见金属单质,且A与B溶液能够反应,则其化学方程式是:
2NaOH+2H2O+2Al=2NaAlO2+3H2↑
2NaOH+2H2O+2Al=2NaAlO2+3H2↑
;
(4)若A是一种常见的化肥,式量为79,且E与F生成G时有白烟产生,则A的化学式
NH4HCO3
NH4HCO3
,G的电子式是:
;
(5)若A是一种溶液,只可能含有H
+.NH
4+、Mg
2+、Fe
3+、Al
3+、CO
32-、SO
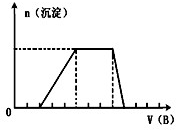
42-中的某些离子,当向该溶液中加入B溶液时发现生成沉淀的物质的量随B溶液的体积变化如图所示,由此可知,该溶液中肯定含有的离子是
H+、NH4+、Al3+、SO42-
H+、NH4+、Al3+、SO42-
(微粒次序按摩尔质量从小到大,下同),物质的量浓度之比为
2:3:1:4
2:3:1:4
.


 (4)若A是一种常见的化肥,式量为79,且E与F生成G时有白烟产生,则A的化学式
(4)若A是一种常见的化肥,式量为79,且E与F生成G时有白烟产生,则A的化学式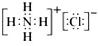
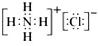
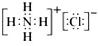 .
.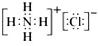 .
.

 阅读快车系列答案
阅读快车系列答案