
| A.该元素为Mn元素 | B.该元素原子核外有4个能层 |
| C.该元素原子最外层共有7个电子 | D.该元素属于d区元素 |
 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案科目:高中化学 来源:不详 题型:填空题

 键的具体类型(即参与成键的原子轨道)
键的具体类型(即参与成键的原子轨道) 查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.144 62Sm与150 62Sm互为同位素 | B.144 62Sm与150 62Sm的质量数相同 |
| C.144 62Sm与150 62Sm是同一种核素 | D.144 62Sm与150 62Sm的中子数均为62 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.电子的运动与行星相似,围绕原子核在固定的轨道上高速旋转 |
| B.分子中键能越大,键长越长,则分子越稳定 |
| C.含有π键的化合物与只含σ键的化合物的化学性质不同 |
| D.元素周期表中位于金属和非金属分界线附近的元素属于过渡元素 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
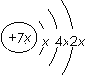 , b与c形成化合物的电子式为
, b与c形成化合物的电子式为  。下列比较中正确的是( )
。下列比较中正确的是( )| A.原子半径:a>c>d>b | B.非金属性 b>d>c |
| C.原子序数:d>a>c>b | D.最高价含氧酸的酸性c>d>a |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 与Y相邻,则D的离子
与Y相邻,则D的离子 结构示意图是 ;D与E能形成
结构示意图是 ;D与E能形成 一种非极性分子,该分子的结构式为 ;D所在族元素的氢化物中,沸点最低的是 。
一种非极性分子,该分子的结构式为 ;D所在族元素的氢化物中,沸点最低的是 。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
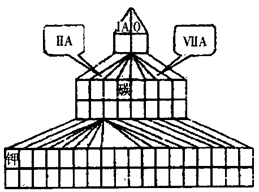
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 种粒子反应后生成一种中性分子,反应的离子方程式是 。
种粒子反应后生成一种中性分子,反应的离子方程式是 。查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com