
| A. | 化学反应除了生成新物质外,还伴随着能量的变化 | |
| B. | 放热反应不需加热就能发生 | |
| C. | 需要加热才能发生的反应不一定是吸热反应 | |
| D. | 化学反应是放热还是吸热,取决于反应物和生成物所具有的总能量的相对高低 |
分析 A.化学反应在发生物质变化的同时还伴随着能量的变化;B.放热反应有的需加热,有的不需加热;C.有的放热反应需要高温条件发生;D.反应放热或吸热的能量变化是有反应物和生成物的焓值差决定,即焓变决定反应热量变化.
解答 解:A.化学反应在发生物质变化的同时还一定伴随着能量的变化,故A正确;B.放热反应有的需加热,有的不需加热,如铝热反应是放热反应,但需要加热,故B错误;C.有的放热反应需要高温条件发生,如铝热反应是放热反应,但需要加热,故C正确;D.反应放热或吸热的能量变化是有反应物和生成物的焓值差决定,即焓变决定反应热量变化,故D正确;故选B.
点评 本题考查化学反应与能量变化,题目难度不大,注意相关基础知识的积累,易错点为B,注意相关概念的理解.


 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:高中化学 来源: 题型:选择题
| A. | 石油的组成元素主要是碳和氧,同时还含有少量的硫、氢、氮等 | |
| B. | 煤是由有机物和无机物所组成的复杂的混合物,煤中含量最高的元素是氢 | |
| C. | 甲烷在一定条件下可被氧化,生成的混合气体在催化剂和一定压强、温度下能合成甲醇(CH3OH) | |
| D. | 所有烷烃中都存在碳碳单键 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溴苯(苯):蒸馏 | B. | 苯(苯酚):加溴水振荡后,过滤 | ||
| C. | 乙烷(乙烯):溴水,洗气 | D. | 苯(溴):稀NaOH溶液,分液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 待提纯的物质 | 选用试剂 | 操作的方法 |
| A | FeCl2溶液(FeCl3溶液) | 铁粉 | 过滤 |
| B | Al2O3(Fe2O3) | NaOH溶液和CO2 | 溶解、过滤、过滤 |
| C | Cl2(HCl) | 饱和食盐水 | 洗气 |
| D | Fe(OH)3胶体(NaCl溶液) | 水 | 渗析 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| X | Y | ||
| W | Z | ||
| T |
| A. | T元素的单质具有半导体的特性,T与Z元素可形成化合物TZ4 | |
| B. | 物质WY2、W3X4、WZ4均有熔点高、硬度大的特性 | |
| C. | 由X、Y和氢三种元素形成的化合物中只有共价键 | |
| D. | X、Y、Z三种元素氢化物的沸点依次升高 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 时间/min | CO | Zn | CO2 |
| 0 | 0.11 | 0 | 0 |
| 2 | 0.10 | 0.01 | 0.01 |
| 3 | 0.01 | 0.10 | 0.10 |
| 4 | 0.01 | 0.10 | 0.10 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
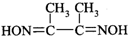 是检验Ni2+的灵敏试剂.
是检验Ni2+的灵敏试剂.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com