


 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 ② (CH3)3COH
② (CH3)3COH 查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
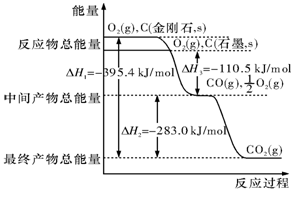
 O2(g)
O2(g) CO(g) ΔH1 = —110.5 kJ/mol
CO(g) ΔH1 = —110.5 kJ/mol O2(g)
O2(g) CO2(g) ΔH2 = —283.0 kJ/mol
CO2(g) ΔH2 = —283.0 kJ/mol CO2(g)的反应热为( )
CO2(g)的反应热为( )| A.172.5 kJ/mol | B.—172.5 kJ/mol | C.393.5 kJ/mol | D.—393.5 kJ/mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.等质量的硫蒸气和硫固体分别完全燃烧,后者放出的热量多 |
| B.由C(金刚石) = C(石墨) ΔH= -1.9 kJ·mol-1可知,金刚石比石墨稳定 |
| C.在101 Kpa时,2 g H2完全燃烧生成液态水,放出285.8 kJ热量,氢气燃烧的热化学方程式为:2 H2(g)+O2(g) =" 2" H2O(l) ΔH =" +285.8" kJ·mol-1 |
| D.稀溶液中:H+(aq) + OH-(aq) = H2O(l) ΔH = -57.3 kJ·mol-1,若将含0.5 mol H2SO4的浓溶液与含1 mol NaOH的溶液混合,放出的热量大于57.3 kJ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.已知NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)△H=-57.3 kJ·mol-1,则含40.0 g NaOH的稀溶液与稀醋酸完全中和,放出小于57.3 kJ的热量 |
| B.已知2H2(g)+O2(g)=2H2O(g)△H=-483.6 kJ·mol--1,则氢气的燃烧热为241.8 kJ·mol-1 |
| C.已知2C(s)+2O2(g)=2CO2(g)△H=a、2C(s)+O2(g)=2CO(g)△H=b,则a>b |
| D.已知P (白磷,s)=P (红磷,s)△H<0,则白磷比红磷稳定 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.乙炔的燃烧热为1256kJ/mol |
| B.若转移10mol电子,则消耗2.5mol O2 |
| C.若生成2mol液态水,则△H=-2512kJ/mol |
| D.若形成4mol碳氧共用电子对,则放出的热量为2512kJ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com