
【题目】下列关于有机化合物的说法正确的是
A. (CH3)3C-CH=CH2与氢气完全反应后,生成2,2,3-三甲基戊烷
B. 工业上由乙烯制乙醇、苯制环己烷均属于加成反应
C. C5H11Cl的同分异构体有3种
D.  分子中所有碳原子一定在同一平面上
分子中所有碳原子一定在同一平面上
【答案】B
【解析】
A、根据加成产物的碳链结构为 去命名;
去命名;
B、根据加成反应的特点答题;
C、先写出C5H12的同分异构体有3种,再写出每种异构体的一氯代物的异构体;
D、苯环上的碳及与6 个碳相连的原子共面。
A. (CH3)3C-CH=CH2与氢气完全反应后,加成产物的碳链结构为 ,系统命名为2,2-二甲基丁烷,故A错误;
,系统命名为2,2-二甲基丁烷,故A错误;
B、乙烯与水在催化剂加热的条件下发生加成反应生成乙醇,同理苯和氢气在一定条件下发生加成反应生成环己烷,故B正确;
C、同分异构体是具有相同的分子式不同结构的化合物的互称, C5H12的同分异构体有3种:![]() 、
、![]() 、
、![]() ,
,![]() 分子中有3种化学环境不同的H原子,其一氯代物有3种;CH3CH2CH(CH3)CH3分中有4种化学环境不同的H原子,其一氯代物有4种;
分子中有3种化学环境不同的H原子,其一氯代物有3种;CH3CH2CH(CH3)CH3分中有4种化学环境不同的H原子,其一氯代物有4种;![]() 分子中只有1种化学环境的H原子,其一氯代物有1种;故C5H11Cl的同分异构体有8种,故C错误;
分子中只有1种化学环境的H原子,其一氯代物有1种;故C5H11Cl的同分异构体有8种,故C错误;
D.如图所示, 1、2、3、4号碳原子共线,同理3、4、5、6号碳 C原子也共线,所以1、2、3、4、5、6号碳原子共线。所以一定在同一平面的碳原子有11个,故D错误。
1、2、3、4号碳原子共线,同理3、4、5、6号碳 C原子也共线,所以1、2、3、4、5、6号碳原子共线。所以一定在同一平面的碳原子有11个,故D错误。
故选B。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】t℃ 时,将3mol A和1molB气体通入体积为2L的密闭容器中(容积不变),发生如下反应:3A(g) + B(g) ![]() xC(g)2min时反应达到平衡状态(温度不变),剩余了0.8molB,并测得C的浓度为0.4mol/L,请填写下列空白:
xC(g)2min时反应达到平衡状态(温度不变),剩余了0.8molB,并测得C的浓度为0.4mol/L,请填写下列空白:
(1)从开始反应至达到平衡的状态,生成C平均反应速率为__________。
(2)x=__________;平衡常数K=____________。
(3)若继续向原混合物的容器中通入少量氦气(设氦气和A、B、C都不反应)后,化学平衡(填字母)____。
A、向正反应方向移动 B、向逆反应方向移动 C、平衡不移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组反应,最终一定能得到白色沉淀的是( )
A.向CaCl2溶液中通入少量CO2
B.向CuSO4溶液中加入足量NaOH溶液
C.向FeCl2溶液中加入足量NaOH溶液
D.向MgSO4溶液中加入足量NaOH溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钒(23V)是我国的丰产元素,广泛应用于催化及钢铁工业,有“化学面包”、金属“维生素”之称。回答下列问题:
(1)钒原子的核外电子排布式为________________,在元素周期表中的位置为______。
(2)V2O5常用作SO2转化为SO3的催化剂。基态S原子电子占据最高能级的电子云轮廓为________形;气态SO3以单分子形式存在,其分子的立体构型为_______形;固体SO3的三聚体环状结构如图所示,该结构中S—O键长有a、b两类,b的键长大于a的键长的原因为______________。

(3)V2O5溶解在NaOH溶液中,可得到钒酸钠(Na3VO4),该盐阴离子中V的杂化轨道类型为___________;也可得到偏钒酸钠,其阴离子呈如图所示的无限链状结构,则偏钒酸钠的化学式为_____________。

(4)钒的某种氧化物晶胞结构如图所示。该氧化物的化学式为__________,若它的晶胞参数为x nm,则晶胞的密度为__________ g/cm3。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钛酸钡的热稳定性好,介电常数高,在小型变压器、话筒和扩音器中都有应用。钛酸钡晶体的晶胞结构示意图如图所示,它的化学式是

A. BaTi8O12
B. BaTiO3
C. BaTi2O4
D. BaTi4O6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A为金属单质,下列物质相互转化如图所示:

试回答:
(1)写出B的化学式____,D的化学式__________。
(2)写出由E转变成F的化学方程式____。
(3)向G溶液加入A的有关离子反应方程式______________________。
(4)某同学取B的溶液酸化后加入碘化钾淀粉溶液,在空气中放置一会儿变为蓝色,写出与上述变化过程相关的离子方程式____________,______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】随着现代工业的发展,二氧化碳污染的处理成为科学研究的重点,回答下列问题:
I.有人提出利用H2还原CO2使其转化为有机化工的主要原料乙烯。
(1)查阅资料:H2的燃烧热为285.8kJ/mol,C2H4的燃烧热为l41lkJ/mol,lmolH2O(1)转化为H2O(g)需吸收44kJ的热量。则反应6H2(g)+2CO2(g) ![]() C2H4(g)+4H2O(g)
C2H4(g)+4H2O(g)
△H=___________kJ/mol。
(2)下图是探究不同温度对CO2的转化率和催化剂的催化效率影响的示意图。

①生产中通常选用的温度最好是___________,理由是___________。
②图中表示的化学平衡常数:M___________N(填>、=、<)
③250℃时,在2L密闭容器中分别充入6molH2和2 molCO2,到达平衡时体系中C2H4的体积分数为___________。
Ⅱ.CO在一定条件下,能与H2合成二甲醚:2CO2(g)+6H2(g)![]() CH3OCH3(g)+3H2O(g)。
CH3OCH3(g)+3H2O(g)。
(1)在1L的密闭容器中分别充入2.5molH2与 bmol CO2发生反应,在不同温度下达到平衡状态时测得实验数据如下表:

①到达平衡时若升高温度,则上述平衡___________方向移动(填“正反应”或“逆反应”)。
②转化率:x___________y(填>、=、<)
(2)新型高效的二甲醚燃料电池工作时总反应式:CH3OCH3+3O2=2CO2+3H2O。
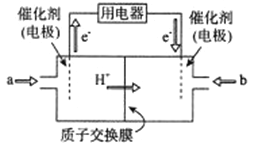
①该电池的负极是___________(填a或b),负极电极反应式为___________;
②利用该电池冶铝,若制得金属铝54g理论上消耗二甲醚___________g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外兴趣小组对H2O2的分解速率做了如下实验探究。
(1)下表是该小组研究影响过氧化氢(H2O2)分解速率的因素时采集的一组数据:
用10 mL H2O2制取150 mL O2所需的时间
浓度 时间(秒) 反应条件 | 30%H2O2 | 15%H2O2 | 10%H2O2 | 5%H2O2 |
(Ⅰ)无催化剂、不加热 | 几乎 不反应 | 几乎 不反应 | 几乎 不反应 | 几乎 不反应 |
(Ⅱ)无催化剂、加热 | 360 | 480 | 540 | 720 |
(Ⅲ)MnO2催化剂、加热 | 10 | 25 | 60 | 120 |
该小组在设计方案时,考虑了浓度、a:___________b:___________等因素对过氧化氢分解速率的影响。
②从上述影响H2O2分解速率的因素a和b中任选一个,说明该因素对该反应速率的影响:_____________。
(2)将质量相同但颗粒大小不同的MnO2分别加入到5 mL 5%的双氧水中,并用带火星的木条测试。测定结果如下:
催化剂 (MnO2) | 操作情况 | 观察结果 | 反应完成所需的时间 |
粉末状 | 混合不振荡 | 剧烈反应,带火星的木条复燃 | 3.5分钟 |
块状 | 反应较慢,火星红亮但木条未复燃 | 30分钟 |
①写出H2O2发生反应的化学方程式:______________________。
②实验结果说明催化剂作用的大小与________________有关。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com