
【题目】一种形状像蝴蝶结的有机分子Bowtiediene,其形状和结构如图所示,下列有关该分子的说法中错误的是

A.1 mol 该物质彻底燃烧需要6 mol O2
B.三氯代物只有一种
C.该分子中所有碳原子在同一平面内
D.与其互为同分异构体,且官能团只含碳碳三键的链烃有两种
【答案】C
【解析】
该题要用已经学过的烃类的性质来类比没有学过的烃类物质,由结构图可以数出该物质一共有5个碳原子,两个环和两个氢键构成4个不饱和度,所以氢原子的数量为![]() 个,所以分子式为
个,所以分子式为![]() ;据此来解题即可。
;据此来解题即可。
A.由分子式![]() 可知,完全燃烧时每mol碳原子消耗1mol氧气,每mol氢原子消耗0.25mol氧气,因此完全燃烧一共需要6mol氧气,A项正确;
可知,完全燃烧时每mol碳原子消耗1mol氧气,每mol氢原子消耗0.25mol氧气,因此完全燃烧一共需要6mol氧气,A项正确;
B.该选项可以看成“在四个氢里面选一个不被取代,另外三个都要被氯取代,有几种选法”,而该分子上的四个氢是完全等效的,因此只有一种选法,也就是一种三氯代物,B项正确;
C.该分子中间的碳原子是sp3杂化,而sp3杂化不可能形成一个平面,C项错误;
D.该烃的分子式为![]() ,分子中有4个不饱和度,若按题目要求只能是碳碳三键,则该物质为戊二炔,戊二炔有1,3-戊二炔和1,4-戊二炔两种,D项正确;
,分子中有4个不饱和度,若按题目要求只能是碳碳三键,则该物质为戊二炔,戊二炔有1,3-戊二炔和1,4-戊二炔两种,D项正确;
答案选C。


科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F是原子序数依次递增的前四周期元素。A是宇宙中含量最丰富的元素;D与E同主族,且E的原子序数是D的两倍;B与D组成的化合物是一种温室气体;C元素原子最外层P能级比S能级多1个电子;F原子的最外层电子数与A相同,其余各层均充满。据此回答下列问题。
(1)F元素形成的高价基态离子的核外电子排布式为__________。
(2)E的一种具有强还原性的氧化物分子的VSEPR模型为__________。
(3)C、D、E元素的第一电离能由大到小的顺序是__________。(用元素符号表示)
(4)A和D形成的18电子化合物难溶于BE2,其理由是__________,此化合物还可将碱性工业废水中的CN-氧化为碳酸盐和氨,相应的离子方程式为__________
(5)C有多种氧化物,其中甲的相对分子质量最小。在一定条件下,2L甲气体与0.5L氧气相混合,若该混合气体被足量的NaOH溶液完全吸收后没有气体残留,所生成的含氧酸盐的化学式是__________。
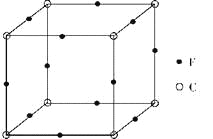
(6)F与C形成化合物的晶胞如图所示,该化合物的化学式为_____________,C离子的配位数是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
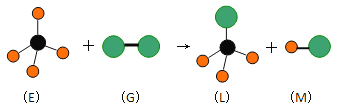
【题目】已知最简单的有机物E和直线型分子G在光照条件下反应,生成四面体型分子L和直线型分子M(组成G分子的元素为第三周期的元素),如下图。则下列判断错误的是
A. 常温常压下,E是一种无色无味的气体
B. 上述反应类型是加成反应
C. 在光照条件L能与 G继续发生与上述类似的反应
D. 上述反应类型是取代反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能证明乙烯分子里含有一个碳碳双键的事实是( )
A.乙烯分子里碳氢原子个数之比为1∶2
B.乙烯完全燃烧生成的CO2和H2O的物质的量相等
C.乙烯能使酸性KMnO4溶液褪色
D.乙烯易与溴水发生加成反应,且1mol乙烯完全加成消耗1mol溴单质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】辉铜矿主要成分为Cu2S,软锰矿主要成分为MnO2,它们都含有少量SiO2、Fe2O3等杂质。工业上综合利用这两种矿物制备硫酸锰和碱式碳酸铜的主要工艺流程如下:
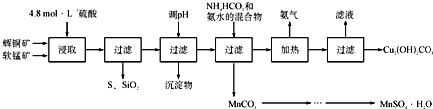
已知:①MnO2能将金属硫化物中的硫氧化为单质硫;
②[Cu(NH3)4]SO4常温稳定,在热水中会分解生成NH3;
③部分金属阳离子生成氢氧化物沉淀的pH范围如下表所示(开始沉淀的pH按金属离子浓度为1.0molL-1计算):
开始沉淀的pH | 沉淀完全的pH | |
Fe 3+ | 1.1 | 3.2 |
Mn2+ | 8.3 | 9.8 |
Cu2+ | 4.4 | 6.4 |
(1)酸浸时,为了提高浸取率可采取的措施有____________________(任写一点);
(2)调节浸出液pH的范围为____________,其目的是_______________________;
(3)本工艺中可循环使用的物质是____________________(写化学式).
(4)在该工艺的“加热驱氨”环节,若加热的温度较低或过高,都将造成_________________的结果;
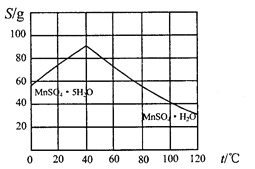
(5)碳酸锰在一定条件下可得硫酸锰溶液,试根据如下曲线图示,现由硫酸锰溶液制备MnSO4·H2O的实验方案为____________________。
(6)用标准BaCl2溶液测定样品中MnSO4H2O质量分数时,发现样品纯度大于100%(测定过程中产生的误差可忽略),其可能原因有_________________(任写一种)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示的装置,C、D、E、F、X、Y都是惰性电极。将电源接通后,向(乙)中滴入酚酞溶液,在F极附近显红色。则下列说法正确的是( )

A.电源B极是正极
B.(甲)(乙)装置的C、D、E、F电极均有单质生成,其物质的量之比为1∶2∶2∶1
C.欲用(丙)装置给铜镀银,H应该是Ag,电镀液是AgNO3溶液
D.装置(丁)中Y极附近红褐色变深,说明氢氧化铁胶粒带正电荷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ、在水的电离平衡中,c(H+)和 c(OH-)的关系如图所示:
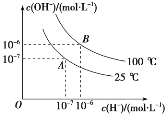
(1)100 ℃时,若向水中滴加盐酸,___(填“能”或“不能”)使体系处于 B 点状态。
(2)25 ℃时,将 pH=9 的 NaOH 溶液与 pH=4 的硫酸溶液混合,所得混合溶液的 pH=7,则 NaOH 溶液与硫酸溶液的体积比为___。
(3)100 ℃时,若盐酸中c(H+)=5×10-5 mol·L-1,则由水电离产生的 c(H+)=____。
Ⅱ、已知在 25 ℃时,醋酸、次氯酸、碳酸和亚硫酸的电离平衡常数分别为醋酸K=1.75×10-5,次氯酸 K=2.95×10-8,碳酸 K1=4.30×10-7 ,K2=5.61×10-11,亚硫酸K1=1.54×10-2,K2=1.02×10-7
(4)写出碳酸的第一级电离平衡常数表达式K1=___。
(5)在相同条件下,等浓度的 CH3COONa、NaClO、Na2CO3、NaHCO3、Na2SO3 和 NaHSO3 溶液中碱性最强的是_____。等浓度的 Na2CO3 和 NaHCO3 的混合溶液中各离子浓度大小顺序为______。
(6)若保持温度不变,在醋酸溶液中通入少量 HCl(g),下列量会变小的是_____(填字母序号,下同)。
a.c(CH3COO-) b.c(H+) c.醋酸的电离平衡常数 d.c(CH3COOH)
(7)下列离子方程式中错误的是_____。
a 少量 CO2 通入次氯酸钠溶液中:CO2+H2O+ClO-=HCO![]() +HClO
+HClO
b 少量 SO2 通入次氯酸钙溶液中:Ca2++2ClO-+SO2+H2O=CaSO3↓+2HClO
c 过量 CO2 通入澄清石灰水中:CO2+OH-=HCO![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组将下列装置按如图连接,C、D、E、F、X、Y都是惰性电极,甲、乙、丙 中电解质溶液含溶质均为 1 mol。将电源接通后,向乙中滴入酚酞溶液,在 F 极附近显红色。
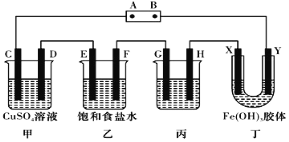
试回答下列问题:
(1)电源 A 极的名称是 ________。
(2)当电路中通过 4 mole-时,要使甲中溶液种类和浓度均复原,可向电解后溶液中加入__________(填某一种物质的化学式和物质的量)。
(3)乙装置中电解反应的总化学方程式为 __________________ 。
(4)若要在丙装置中实现铁器上镀银,银在 _____(填 G 或 H)级。
(5)装置丁中的现象是 _________________________。
(6)若电源用碱性氢氧燃料电池代替,则该电池正极的电极反应式为 ______________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汉黄芩素对肿瘤细胞的杀伤有独特作用,其结构如图所示,下列有关叙述正确的是( )
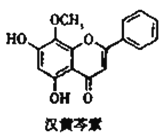
A. 汉黄芩素的分子式为C16H14O5
B. 1mol该物质与NaOH溶液反应,可消耗2molNaOH
C. 1mol该物质与溴水反应,最多消耗1molBr2
D. 该物质可发生取代、加成、缩聚、消去反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com