

 消去反应
消去反应 取代反应.
取代反应. 分析 (1)①属于芳香烃的有机物只含C、H两种元素,且含有苯环或稠环;
②属于醇类的物质应含有羟基,且羟基与苯环不直接相连;
③根据醛基的结构简式判断;
(2)①实验室用乙醇发生消去反应制取乙烯;
②苯酚与浓溴水反应生成三溴苯酚沉淀和溴化氢.
解答 解:(1)①属于芳香烃的有机物只含C、H两种元素,且含有苯环或稠环,题中只有⑨符合,
故答案为:⑨;
②属于醇类的物质应含有羟基,且羟基与苯环不直接相连,题中只有①符合,
故答案为:①;
③醛基的结构简式为 ,则题中⑦⑧含有醛基,
,则题中⑦⑧含有醛基,
故答案为:⑦⑧;
(2)①实验室制乙烯的化学方程式为: ,该反应为消去反应,
,该反应为消去反应,
故答案为: 、消去反应;
、消去反应;
②苯酚和浓溴水反应生成三溴苯酚和溴化氢,反应方程式为: ,该反应为取代反应,
,该反应为取代反应,
故答案为: 取代反应.
取代反应.
点评 本题考查有机物分类、有机反应方程式书写,题目难度不大,明确常见有机物组成及分类方法为解答关键,注意掌握常见有机物结构与性质,试题培养了学生的灵活应用能力.


科目:高中化学 来源: 题型:选择题
| A. | 正反应速率等于逆反应速率 | B. | 各物质的浓度不再改变 | ||
| C. | 反应停止了 | D. | 该反应达到最大限度 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2Q1+Q2>Q3 | B. | Q1+Q2>2Q3 | C. | 2Q1+Q2<4Q3 | D. | 2Q1+Q2<2Q3 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 邻二甲苯有二种不同结构 | |
| B. | 高温下甲烷能分解 | |
| C. | 乙烯能使溴水和酸性高锰酸钾溶液褪色,其褪色原理相同 | |
| D. | 等质量的聚乙烯、乙烯分别充分燃烧,聚乙烯所耗氧气的物质的量多 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②③ | B. | ②④ | C. | ①③ | D. | ①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
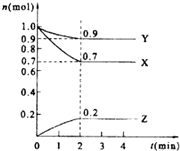 某温度时.在2L的密闭容器中,X、Y、Z(均为气体)三种物质的量随时间的变化曲线如图所示.
某温度时.在2L的密闭容器中,X、Y、Z(均为气体)三种物质的量随时间的变化曲线如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只有x+2 | B. | 可能是x+2 或x+10或x+24 | ||
| C. | 可能是x+24 | D. | 可能是x+2或x+12或x+26 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,20 g D2O分子中所含中子数为10 NA | |
| B. | 0.1 mol FeCl3水解生成的Fe(OH)3胶粒数为0.1 NA | |
| C. | 将lmol Cl2通入水中,HC1O、Cl-、C1O-粒子数之和为2 NA | |
| D. | 常温常压下,11.2 L CO2 与足量Na2O2反应转移的电子数为0.5 NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com