
甲酸钠广泛用作催化剂和稳定合成剂,印染行业的还原剂,还可用于生产保险粉、草酸和甲酸。用电石炉废气(CO 75~90%,以及少量CO2、H2S、N2、CH4等)其合成部分工艺流程如下:

(1)上述工艺用碱液洗涤的目的是 ,可能发生的反应有 (列举两例)。
(2)上述合成工艺中采用循环喷射吸收合成,其目的是 ;最后排空的尾气主要成分是 。
(3) 合成时,得到的HCOONa溶液溶质质量分数约为5%,合成塔反应液中分离出HCOONa·2H2O的主要步骤有 、 、 ,再经洗涤干燥得到。
(4) 甲酸钠高温时分解制取草酸钠的化学方程式为 。
(5) 在甲酸钠、氢氧化钠混合溶液中通入二氧化硫气体,可得到重要工业产品保险粉(Na2S2O4)同时产生二氧化碳,该反应离子方程式为 。
 智慧小复习系列答案
智慧小复习系列答案科目:高中化学 来源:2015-2016学年福建省高二上学期期中(理)化学试卷(解析版) 题型:选择题
根据电子排布的特点,Br在周期表属于
A.s区 B.p区 C.d 区 D.ds区
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高二上学期第二次月考化学试卷(解析版) 题型:选择题
下列仪器中没有零刻度的是( )
A.温度计 B.量筒 C.滴定管 D.托盘天平游码标尺
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河南省高一上学期期中考试化学试卷(解析版) 题型:选择题
将饱和氯化铁溶液分别滴入下列液体中,能形成胶体的是
A.冷水 B.氯化钠溶液 C.沸水 D.氢氧化钠溶液
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河南省高二上学期期中考试化学试卷(解析版) 题型:选择题
下列对化学反应的认识正确的是 ( )
A.化学反应过程中,分子的种类和数目一定发生改变
B.如果某化学反应的ΔH和ΔS均小于0,则反应一定能自发进行
C.化学反应过程中,一定有化学键的断裂和形成
D.反应物的总焓大于反应产物的总焓时,ΔH>0
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西省、高安二中高二上期中联考化学试卷(解析版) 题型:选择题
“低碳经济”是以低能耗、低污染、低排放为基础的可持续发展经济模式。下列说法与“低碳经济”不符合的是( )
A.大力研发新型有机溶剂替代水作为萃取剂
B.加强对煤、石油、天然气等综合利用的研究,提高燃料的利用率
C.利用CO2合成聚碳酸酯类可降解塑料,实现“碳”的循环利用
D.使用甲醇、乙醇混合型汽油可以减少对大气的污染
查看答案和解析>>
科目:高中化学 来源:2016届河北省高三上学期12月月考化学试卷(解析版) 题型:简答题
(2011·浙江,27)某研究小组在实验室探究氨基甲酸铵(NH2COONH4)分解反应平衡常数和水解反应速率的测定。
(1)将一定量纯净的氨基甲酸铵固体置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:NH2COONH4(s) 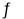 2NH3(g)+CO2(g)
2NH3(g)+CO2(g)
实验测得不同温度下的平衡数据列于下表:
温度/℃ | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
平衡总压强/kPa | 5.7 | 8.3 | 12.0 | 17.1 | 24.0 |
平衡气体总浓 度/mol·L-1 | 2.4×10-3 | 3.4×10-3 | 4.8×10-3 | 6.8×10-3 | 9.4×10-3 |
①可以判断该分解反应已经达到平衡的是_______________ 。
A.2v(NH3)=v(CO2)
B.密闭容器中总压强不变
C.密闭容器中混合气体的密度不变
D.密闭容器中氨气的体积分数不变
②根据表中数据,列式计算25.0 ℃时的分解平衡常数:________。
③取一定量的氨基甲酸铵固体放在一个带活塞的密闭真空容器中,在25.0 ℃下达到分解平衡。若在恒温下压缩容器体积,氨基甲酸铵固体的质量_________________ (填“增加”,“减少”或“不变”)。
④氨基甲酸铵分解反应的焓变ΔH_______________0(填“>”、“=”或“<”),熵变ΔS________________0(填“>”、“=”或“<”)。
(2)已知:NH2COONH4+2H2O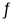 NH4HCO3+NH3·H2O
NH4HCO3+NH3·H2O
该研究小组分别用三份不同初始浓度的氨基甲酸铵溶液测定水解反应速率,得到c(NH2COO-)随时间的变化趋势如下图所示。
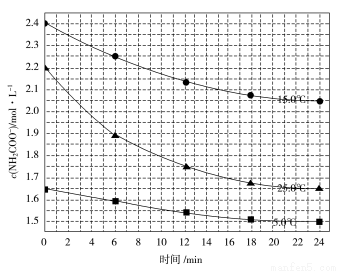
⑤计算25.0 ℃时,0~6 min氨基甲酸铵水解反应的平均速率:________。
⑥根据图中信息,如何说明该水解反应速率随温度升高而增大:______________ _______________________________。
查看答案和解析>>
科目:高中化学 来源:2016届河南省三门峡市高三上学期第二次月考化学试卷(解析版) 题型:选择题
将ag镁铝合金投入到x mL 2mol/L的盐酸中,金属完全溶解后,再加入y mL 1mol/L的氢氧化钠溶液,得到的沉淀量最大,质量为(a+1.7)g。下列说法不正确的是 ( )
A.2x=y
B.x=2y
C.沉淀是Mg(OH)2和Al(OH)3的混合物
D.镁铝合金与盐酸反应转移电子总数为0.1NA
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广东省高二上第三次月考化学试卷(解析版) 题型:选择题
反应2SO2+O2 2SO3在密闭容器中进行。下列关于该反应的说法错误的是
2SO3在密闭容器中进行。下列关于该反应的说法错误的是
A.升高温度能加快反应速率 B.使用恰当的催化剂能加快反应速率
C.增大O2的浓度能加快反应速率 D.SO2与O2能100%转化为SO3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com