
已知AgI为黄色沉淀,AgCl为白色沉淀,25 ℃时,AgI饱和溶液中c(Ag+)=1.22×10-8 mol·L-1,AgCl饱和溶液中c(Ag+)=1.30×10-5 mol·L-1。若在5 mL含有KCl和KI浓度均为0.01 mol·L-1的混合溶液中,滴加8 mL 0.01 mol·L-1的AgNO3溶液,则下列叙述中不正确的是( )
A.溶液中所含溶质的离子浓度大小关系为c(NO )>c(K+)>c(Cl-)>c(I-)>c(Ag+)
)>c(K+)>c(Cl-)>c(I-)>c(Ag+)
B.溶液中先产生的是AgI沉淀
C.AgCl的Ksp的数值为1.69×10-10
D.若在AgI悬浊液中滴加KCl溶液、黄色沉淀可能转变成白色沉淀
解析:本题考查了难溶电解质的电离平衡、Ksp的有关计算、离子浓度大小比较等,意在考查考生的理解能力及计算能力。根据已知条件,若在含有KCl和KI的溶液中加入AgNO3溶液,首先生成AgI沉淀,反应后剩余n(Ag+)=(0.008-0.005) L×0.01 mol·L-1=3×10-5 mol,继续生成AgCl沉淀,反应后剩余n(Cl-)=0.005 L×0.01 mol·L-1-3×10-5 mol=2×10-5 mol,c(Cl-)=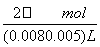 =1.54×10-3 mol/L,悬浊液中c(Ag+)=
=1.54×10-3 mol/L,悬浊液中c(Ag+)=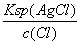 =
=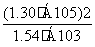 =1.10×10-7(mol·L-1),c(I-)=
=1.10×10-7(mol·L-1),c(I-)=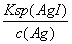 =
=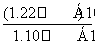 =1.35×10-9,混合溶液中n(K+)=1×10-4 mol,n(NO
=1.35×10-9,混合溶液中n(K+)=1×10-4 mol,n(NO )=0.008 L×0.01 mol·L-1=8.0×10-5 mol,则c(K+)>c(NO
)=0.008 L×0.01 mol·L-1=8.0×10-5 mol,则c(K+)>c(NO ),故c(K+)>c(NO
),故c(K+)>c(NO )>c(Cl-)>c(Ag+)>c(I-),A项错误;AgI比AgCl更难溶,先产生的是AgI沉淀,B项正确;AgCl的Ksp的数值为(1.30×10-5)2=1.69×10-10,C项正确;AgI饱和溶液中c(Ag+)=1.22×10-8 mol·L-1,Ksp(AgCl)=1.69×10-10,当溶液中c(Cl-)≥
)>c(Cl-)>c(Ag+)>c(I-),A项错误;AgI比AgCl更难溶,先产生的是AgI沉淀,B项正确;AgCl的Ksp的数值为(1.30×10-5)2=1.69×10-10,C项正确;AgI饱和溶液中c(Ag+)=1.22×10-8 mol·L-1,Ksp(AgCl)=1.69×10-10,当溶液中c(Cl-)≥ =
=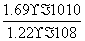 =1.39×10-2(mol·L-1)时,AgI可转化为AgCl,D项正确。
=1.39×10-2(mol·L-1)时,AgI可转化为AgCl,D项正确。
答案:A


科目:高中化学 来源: 题型:
把a、b、c、d四块金属浸入稀硫酸中,用导线两两相连组成原电池,若a、b相连时,a为负极;c、d相连时,电流由d到c;a、c相连时,c极上产生大量气泡;b、d相连时,b上有大量气泡产生,则四种金属的活动性顺序为( )
A.a>b>c>d B. a>c>d>b C.c>a>b>d D.b>d>c>a
查看答案和解析>>
科目:高中化学 来源: 题型:
合金与纯金属制成的金属材料相比,优点是 ( )
①合金的硬度一般比它的各成分金属的大
②一般地,合金的熔点比它的各成分金属的更低
③改变原料的配比、改变生成合金的条件,得到有不同性能的合金
④合金比纯金属的导电性更强
⑤合金比纯金属的应用范围更广泛
A.②③④ B.①②③⑤
C.①②④ D.①②④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
所谓合金,就是不同种金属(也包括一些非金属)在熔化状态下形成的一种熔合物,下表为四种金属的熔、沸点:
| Na | Cu | Al | Fe | |
| 熔点(℃) | 97.5 | 1 083 | 660 | 1 535 |
| 沸点(℃) | 883 | 2 595 | 2 200 | 3 000 |
根据以上数据判断其中不能形成合金的是 ( )
A.Cu和Al B.Fe和Cu
C.Fe 和Na D.Al和Na
和Na D.Al和Na
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,下列溶液的pH或微粒的物质的量浓度关系正确的是( )
A.某物质的溶液中由水电离出的c(H+)=1×10-a mol/L,若a>7,则该溶液的pH一定为14-a
B.某溶液中存在的离子有S2-、HS-、OH-、Na+、H+,则离子浓度的大小关系一定是:c(Na+)>c(S2-)>c(OH-)>c(HS-)>c(H+)
C.pH=3的二元弱酸H2R溶液与pH=11的NaOH溶液混合后,混合液的pH等于7,则反应后的混合液:c(R2-)+c(HR-)=c(Na+)
D.将0.2 mol/L的某一元酸HA溶液和0.1 mol/L NaOH溶液等体积混合后溶液pH大于7,则反应后的混合液:2c(OH-)=2c(H+)+c(HA)-c(A-)
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,pH=3的HA溶液V1 mL与pH=11的KOH溶液V2 mL混合,则下列说法正确的是( )
A.若V1=V2,则反应后溶液的pH一定等于7
B.若反应后溶液呈酸性,则V1一定小于V2
C.若反应后溶液呈酸性,则V1一定大于V2
D.若反应后溶液呈中性,则混合液中一定存在c(H+)+c(OH-)=2×10-7 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
锌烂板液是制作印刷锌板时用稀HNO3腐蚀锌板后得到的废液,主要含Zn(NO3)2和自来水带进的Cl-、Fe3+等杂质离子。某兴趣小组在实验室中由锌烂板液制取ZnSO4·7H2O的步骤如下:
①在锌烂板液中逐渐加入6 mol/L氢氧化钠溶液,用pH试纸检验,直至pH=8;
②过滤后得到粗Zn(OH)2沉淀,用蒸馏水多次洗涤沉淀;
③用2 mol/L硫酸慢慢将洗净的粗Zn(OH)2沉淀溶解,保持一定pH,加热煮沸,趁热过滤,滤液即为ZnSO4溶液;
④在滤液中注入2 mol/L的硫酸,调节pH为2左右,后经相关操作得到ZnSO4·7H2O晶体。
已知:常温下,Fe3+在pH=1.9开始沉淀,pH=3.2沉淀完全;Zn2+在pH=6.4开始沉淀,pH=8.0沉淀完全;Zn(OH)2的化学性质与Al(OH)3相似。
(1)在以上所有步骤中都需要用到的仪器是烧杯、___________。
(2)步骤②的目的是除去________________等杂质离子,检验沉淀是否已洗净的具体操作是________________。
(3)步骤①保持pH=8的目的是________________,步骤④保持pH =2的目的是________________。
(4)步骤③为了除去Fe3+,故保持的pH范围为_____________,加热煮沸的目的是________________。
(5)步骤④中得到ZnSO4·7H2O晶体的操作步骤为____________、________________、过滤、洗涤、干燥。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是
A.发生化学反应时得到电子越多,非金属原子的氧化能力越强
B.金属阳离子被还原后,一定得到该元素的单质
C.核外电子数相同的原子,一定是同种元素的原子
D.能与酸反应的氧化物,一定是碱性氧化物
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是
①久置于空气中的氢氧化钠溶液,加盐酸时有气体产生
②浓硫酸可用于干燥氨气、二氧化氮气体
③SiO2和CO2都是酸性氧化物,都能与强碱溶液反应,但不能与任何酸反应
④玻璃、水泥、水晶项链都是硅酸盐制品
⑤蔗糖炭化的演示实验中,浓硫酸既体现了其强氧化性又体现了其脱水性
A.①④⑤ B.①⑤ C.②③④ D.④⑤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com