
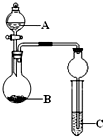
 用下列几个实验,可快速制取实验室所需的少量气体,并进行相关性质实验.(实验装置如图所示)
用下列几个实验,可快速制取实验室所需的少量气体,并进行相关性质实验.(实验装置如图所示)

科目:高中化学 来源: 题型:阅读理解
| ||
| △ |
| ||
| 加入药品 | 不加MnSO4的硫酸 酸化的H2C2O4溶液 |
加少量MnSO4的硫酸 酸化的H2C2O4溶液 |
| 实验现象 (褪色时间)/s |
H2C2O4褪色很慢 (31秒) |
H2C2O4褪色很快(4秒) |
查看答案和解析>>
科目:高中化学 来源:物理教研室 题型:058
(1)气体发生器置于左侧,气体向右方流动,所用仪器与导管依次连接序号为:
( )接( )接( )接( )接( )接( )。

(2)进行实验时的操作如下(每项进行—次):
①从分液漏斗中逐滴把无水酒精加入烧瓶中,并控制反应速度,酒精加完后关闭活塞
②在广口瓶内注入适量水
③待烧瓶冷却到室温后对量筒读数
④把定量的a(mL)无水酒精无损失地倒入分液漏斗中
⑤检查装置的气密性
⑥预先将小块钠块在二甲苯中熔化成小钠珠,冷却后倒入烧瓶中,塞紧橡皮塞
⑦估计反应接近完全,用酒精灯对烧瓶略加微热,使反应完成,再撤灯正确操作的序号是_____________________。
(3)出现下列情况时,对实验结果影响怎样?(用A.偏高,B.偏低,C.无影响的代号答题)
①此反应是放热反应,反应速度太快,有部分乙醇挥发,使实验结果_______________。
②如果无水酒精中混合少量甲醇,使实验结果________________。
③读数时,如果量筒内液面高于广口瓶的液面,使实验结果________________。
(4)如果此实验数据视作标准状况的数据:无水乙醇的密度为r(g×cm-3),a(mL)乙醇反应完全后,量筒内的液面读数为b(mL),则一个乙醇分子中能取代出的氢原子数为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:058
利用乙醇和钠反应来确定乙醇分子中有几个可被置换的H原子是经典的定量实验之一。反应原理:乙醇+钠(足量)→乙醇钠+氢气,所需选用的实验仪器如图(D与F均具有双孔橡皮塞)所示:
(1)气体发生器置于左侧,气体向右方流动,所用仪器与导管依次连接序号为:
( )接( )接( )接( )接( )接( )。

(2)进行实验时的操作如下(每项进行—次):
①从分液漏斗中逐滴把无水酒精加入烧瓶中,并控制反应速度,酒精加完后关闭活塞
②在广口瓶内注入适量水
③待烧瓶冷却到室温后对量筒读数
④把定量的a(mL)无水酒精无损失地倒入分液漏斗中
⑤检查装置的气密性
⑥预先将小块钠块在二甲苯中熔化成小钠珠,冷却后倒入烧瓶中,塞紧橡皮塞
⑦估计反应接近完全,用酒精灯对烧瓶略加微热,使反应完成,再撤灯正确操作的序号是_____________________。
(3)出现下列情况时,对实验结果影响怎样?(用A.偏高,B.偏低,C.无影响的代号答题)
①此反应是放热反应,反应速度太快,有部分乙醇挥发,使实验结果_______________。
②如果无水酒精中混合少量甲醇,使实验结果________________。
③读数时,如果量筒内液面高于广口瓶的液面,使实验结果________________。
(4)如果此实验数据视作标准状况的数据:无水乙醇的密度为r(g×cm-3),a(mL)乙醇反应完全后,量筒内的液面读数为b(mL),则一个乙醇分子中能取代出的氢原子数为_____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com