
��Ԫ�����ڱ�������Ԫ���У�AԪ��ԭ�ӵ�����������������Ӳ�����3����BԪ�صĵ�����AԪ�صĵ��ʻ������ɻ�����B2A2����ɫ���壻CԪ�ص���������AԪ�ص������ӵ��Ӳ�ṹ��ͬ��0.1 mol C�������������ᷴӦ�����ɵ�H2�ڱ�������Ϊ3.36 L��DԪ����CԪ��ͬ���ڣ�D�Ǹ������зǽ����������ķǽ���Ԫ�ء�
(1)��Ԫ�صķ�����A________��B________��C________��D________��
(2)BԪ�صĵ�����AԪ�صĵ��ʻ������ɻ�����B2A2�Ļ�ѧ����ʽΪ____________________________________________��
(3)C������������Ӧˮ������NaOH��Һ��Ӧ�Ļ�ѧ����ʽΪ________________________��
(4)D��ԭ�ӽṹʾ��ͼΪ________����̬�⻯�����ʽΪ________��
(5)���ʵ�����ͬ��C��D�ֱ���������ǿ����Һ��Ӧ������������ʵ���֮����________��
������(1)���������֪��AԪ��ԭ�ӵĺ�������Ų�Ϊ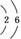 ��AΪO��B2A2ΪNa2O2����BΪNa��Cλ�ڵ�3���ڣ������γɣ�3�۵Ľ���Ԫ�أ���CΪAl��D�ǵ�3�����зǽ����������ķǽ���Ԫ�أ���DΪSi��(5)����2Al��2OH����2H2O===2AlO
��AΪO��B2A2ΪNa2O2����BΪNa��Cλ�ڵ�3���ڣ������γɣ�3�۵Ľ���Ԫ�أ���CΪAl��D�ǵ�3�����зǽ����������ķǽ���Ԫ�أ���DΪSi��(5)����2Al��2OH����2H2O===2AlO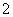 ��3H2����Si��2OH����H2O===SiO
��3H2����Si��2OH����H2O===SiO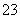 ��2H2������֪2 mol Al��������ǿ����Һ��Ӧ����3 mol H2��2 mol Si��������ǿ����Һ��Ӧ����4 mol H2��
��2H2������֪2 mol Al��������ǿ����Һ��Ӧ����3 mol H2��2 mol Si��������ǿ����Һ��Ӧ����4 mol H2��
�𰸡�(1)O��Na��Al��Si
(2)2Na��O2 Na2O2
Na2O2
(3)Al(OH)3��NaOH===NaAlO2��2H2O
(4) ��SiH4
��SiH4
(5)34


 �ִʾ��ƪϵ�д�
�ִʾ��ƪϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��ѧ������ѧϰ��ѧ����Ҫ���ߣ�����������ʾ���ʱ仯�Ļ�ѧ�����У���ȷ����(����)
A����ⱥ��ʳ��ˮ�������ĵ缫��ӦʽΪ��2Cl����2e��===Cl2��
B������ȼ�ϵ�صĸ�����Ӧʽ��O2��2H2O��4e��===4OH��
C����ͭ����ʱ�����������������Ǵ�ͭ���缫��ӦʽΪ��Cu��2e��===Cu2��
D�����������绯ѧ��ʴ��������Ӧʽ��Fe��2e��===Fe2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
������Һ��Ũ��ˮ��ӽ�������������̵���(����)
A��Ũ���ᡡ������������ B��Ũ����
C��Һ�� D��Ũ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�л������һ���������ܷ���ˮ�ⷴӦ���������л�����Т١����DZ���ĸ��л�������в�ͬ�Ļ�ѧ������ˮ��ʱ�����ѵļ���(����)
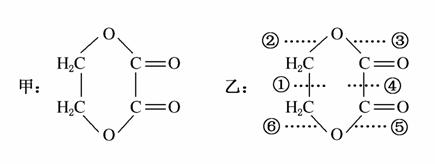
A���٢� B���ۢ�
C���ڢ� D���ڢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����ڽ���Ԫ�ؼס�����Ԫ�����ڱ��е����λ�����±���ʾ�������ж���ȷ����(����)
| �� | �� | |
| �� | �� | �� |
A.ԭ�Ӱ뾶������������
B�������ԣ��ף���
C������������ԣ�����������
D���������������ף���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���ֶ�����Ԫ�ص�ԭ�Ӱ뾶����Ҫ���ϼ����±���
| Ԫ�ش��� | X | Y | Z | W |
| ԭ�Ӱ뾶/pm | 160 | 143 | 70 | 66 |
| ��Ҫ���ϼ� | ��2 | ��3 | ��5����3����3 | ��2 |
����������ȷ����(����)
A. X��YԪ�صĽ�����X��Y
B��һ�������£�Z������W�ij�������ֱ������ZW2
C. Y������������ˮ����������ϡ��ˮ
D��X������������ˮ��������Z������������ˮ������кͷ�Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����Ȼ�ѧ����ʽ�Ц�H��ʾ��ȼ���ȼ���ȵ���(����)
A��CO(g)��O2(g)===CO2(g)����H����283 kJ��mol��1
B��CH4(g)��2O2(g)===CO2(g)��2H2O(g)
��H����802.3 kJ��mol��1
C��2H2(g)��O2(g)===2H2O(l)
��H����571.6 kJ��mol��1
D��H2(g)��Cl2(g)===2HCl(g)
��H����184.6 kJ��mol��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���б仯�����У���Ҫ��������������ʵ�ֵ���(����)
A��HCl��H2 B��HCl��FeCl2
C��H2SO4(Ũ)��SO2 D��Fe��Fe2O3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���й����У����ڷ��Է����̵���(����)
A��N2��O2���
B�����¡���ѹ�£�ʯīת��Ϊ���ʯ
C��H2��O2��������H2O
D��C��O2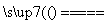 CO2
CO2
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com