
分析 (1)醋酸是弱酸,不完全电离;
(2)醋酸的电离是吸热反应,加水稀释、加入碱、加热都能促进醋酸的电离;
(3)根据Ka=$\frac{[C{H}_{3}CO{O}^{-}]•[{H}^{+}]}{[C{H}_{3}COOH]}$计算;
解答 解:(1)醋酸为弱酸,液中部分电离,电离方程式用可逆符号,电离方程式为CH3COOH?H++CH3COO-,故答案为:CH3COOH?H++CH3COO-;
(2)醋酸的电离是吸热反应,加水稀释、加入碱、加热都能促进醋酸的电离;
a.加入少量0.10mol•L-1的稀盐酸,溶液中氢离子浓度增大,抑制醋酸的电离,则醋酸的电离程度降低,故错误;
b.加入少量冰醋酸,醋酸的电离平衡向正反应方向移动,但醋酸的电离程度降低,故错误;
c.加入少量氯化钠固体,不影响平衡的移动,则不改变醋酸的电离,故错误;
d.醋酸的电离是吸热反应,加热CH3COOH溶液,促进醋酸的电离,则醋酸的电离程度增大,故正确;
e.加入Zn粒,锌能够与氢离子反应,醋酸的电离平衡正向移动,故正确;
f.加入少量0.10mol•L-1的CH3COONa溶液,醋酸根离子浓度增大,抑制醋酸的电离,则醋酸的电离程度减小,故错误;
故答案为:de;
(3)25℃时,在0.5L 0.2mol•L-1的CH3COOH溶液中,有0.01mol的CH3COOH电离成离子,则c(H+)=c(CH3COO-)=$\frac{0.01mol}{0.5L}$=0.05mol/L,
则Ka=$\frac{[C{H}_{3}CO{O}^{-}]•[{H}^{+}]}{[C{H}_{3}COOH]}$=$\frac{0.05×0.05}{0.2-0.05}$=2.22×10-3;
故答案为:2.22×10-3;
点评 本题考查电解质的电离、电离平衡的移动以及电离常数的计算,题目难度中等,侧重于考查学生对基础知识的应用能力.


 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径A>B>D>C | |
| B. | 原子序数d>c>b>a | |
| C. | 离子半径C>D>B>A | |
| D. | 原子结构的最外层电子数目A>B>D>C |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 )是一种食用香料,主要用于配制具有醋栗、桃、草莓、樱桃、可可、巧克力等各种香气浓厚的香精.其中一种合成路线如下:
)是一种食用香料,主要用于配制具有醋栗、桃、草莓、樱桃、可可、巧克力等各种香气浓厚的香精.其中一种合成路线如下:

 +2Cu(OH)2$\stackrel{△}{→}$
+2Cu(OH)2$\stackrel{△}{→}$ +Cu2O↓+2H2O.
+Cu2O↓+2H2O. +(CH3)2CHCH2OH$→_{△}^{浓硫酸}$
+(CH3)2CHCH2OH$→_{△}^{浓硫酸}$ +H2O,反应类型为酯化反应或取代反应.
+H2O,反应类型为酯化反应或取代反应.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3:4 | B. | 1:2 | C. | 2:3 | D. | 3:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 无色溶液中:Al3+、Cu2+、Cl-、SO42- | |
| B. | 含有Na2CO3的溶液:Al3+、Ca2+、Cl-、NO3- | |
| C. | 溶有大量Cl2的溶液:I-、SiO32-、K+、H+ | |
| D. | 25℃时pH<7的溶液:K+、Na+、Fe3+、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
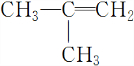 .
. +3HNO3
+3HNO3
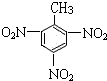 +3H2O;
+3H2O;查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com