
(14分)在工业生产和日常生活中有重要用途。 I.工业上用钛矿石(
,含
等杂质)经过下述反应制得:
其中,步骤②发生的反应为:
(1)净化钛矿石时,是否需要除去杂质FeO? ______ (填“需要”或“不需要”)。
(2) 净化钛矿石时,需用浓氢氧化钠溶液来处理,写出该过程中发生反应的化学方程式: __________________
II. TiO2可通过下述两种方法制备金属钛:
“方法一”是电解TiO2来获得Th将处理过的TiO2作阴极,石墨为阳极,熔融CaO为电解液,用碳块作电解槽池。
(3)阴极反应的电极反应式为__________________
“方法二”是先将TiO2与 Cl2、C反应得到TiCl4,再用镁还原得到TL因下述反应难于发生:
所以不能直接由Ti02和Cl2反应(即氯化反应)来制取TiCl4。当往氯化反应体系中加入碳后,碳与上述反应发生耦合,使得反应在高温条件下能顺利进行。
(4) 己知:
请写出与Cl2、C反应制取TiO4的热化学方程式:____________
(5)从化学平衡的角度解释:往氯化反应体系中加入碳时,氯化反应能顺利进行的原因________________________________________________
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2013届吉林省长春市实验中学高三上学期第一次月考化学试卷(带解析) 题型:填空题
(14分) 卤化物和卤酸盐在工业生产中有着重要的作用。某小组为探究其中一些盐的性质,查阅资料并进行实验。查阅资料如下:
① BrO3- + 6I- + 6H+ = 3I2 + Br-+ 3H2O ② 2BrO3- + I2 = 2IO3- + Br2
③ IO3- + 5I- + 6H+ = 3I2 + 3H2O ④ 2IO3- + 10Br-+ 12H+ = I2 + 5Br2 + 6H2O
实验如下:
| 步骤 | 现象 |
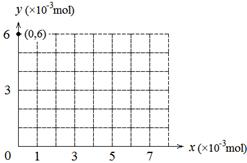
| ⅰ.向盛有30 mL 0.2 mol·L-1 KI溶液的锥形瓶中依次滴入几滴淀粉溶液和足量稀硫酸,再用滴定管逐滴加入KBrO3溶液 | 随着KBrO3溶液滴入,溶液由无色变为蓝色并逐渐加深,最终保持不变 |
| ⅱ.继续向上述溶液中滴入KBrO3溶液 | 溶液的蓝色逐渐褪去 |
查看答案和解析>>
科目:高中化学 来源:2013届江苏省盐城市明达中学高三上学期学情调研考试化学试卷(带解析) 题型:填空题
(14 分)过氧化氢和臭氧都是常见的绿色氧化剂,在工业生产中有着重要的用途。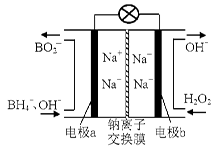
(1)据报道以硼氢化合物NaBH4(B的化合价为+3价)和H2O2作原料的燃料电池,可用作通信卫星电源。负极材料采用Pt/C,正极材料采用MnO2,其工作原理如右图所示。该电池放电时正极的电极反应式为: ;
以MnO2做正极材料,可能是因为 。
(2)火箭发射常以液态肼(N2H4)为燃料,液态过氧化氢
为助燃剂。已知:
N2H4(g) + O2(g) = N2(g) + 2H2O(g) △H =" –" 534 kJ·mol-1
H2O2(l) = H2O(l) + 1/2O2(g) △H =" –" 98.64 kJ·mol-1
H2O(l) = H2O(g) △H=" +" 44kJ·mol-1
则反应N2H4(g) + 2H2O2(l) = N2(g) + 4H2O(g) 的△H= 。
(3)O3 可由臭氧发生器(原理如右图所示)电解稀硫酸制得。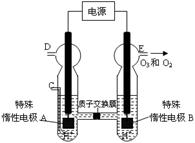
② 图中阴极为 (填“A”或“B”)。
②若C处通入O 2,则A极的电极反应式为: 。
③若C处不通入O 2 ,D、E处分别收集到15.68L和有6.72L气体(标准状况下),则E处收集的气体中O2和O3的体积之比为 (忽略 O 3 的分解)。
(4)新型O3氧化技术对燃煤烟气中的NOx和SO2脱除效果显著,锅炉烟气中的NOx 以上是以NO形式存在的,可发生反应NO(g)+ O3 (g)
以上是以NO形式存在的,可发生反应NO(g)+ O3 (g)  NO2(g)+ O2 (g)。在一定条件下,将NO和O3通入绝热恒容密闭容器中发生上述反应 ,正反应速率随时间变化的示意图(如下图)所示。由图可得出的正确说法是
NO2(g)+ O2 (g)。在一定条件下,将NO和O3通入绝热恒容密闭容器中发生上述反应 ,正反应速率随时间变化的示意图(如下图)所示。由图可得出的正确说法是 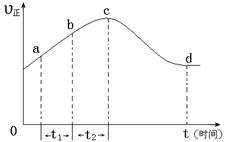
a.反应在c点达到平衡状态
b.反应物浓度:b点小于c点
c.该反应为放热反应
d.Δt1=Δt2时,NO的转化量:a~b段小于b~c段
查看答案和解析>>
科目:高中化学 来源:2012届四川省自贡市高三上学期第一次诊断性考试理综试题(化学部分) 题型:实验题
(14分)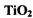 在工业生产和日常生活中有重要用途。 I.工业上用钛矿石(
在工业生产和日常生活中有重要用途。 I.工业上用钛矿石( ,含
,含 等杂质)经过下述反应制得:
等杂质)经过下述反应制得:
其中,步骤②发生的反应为: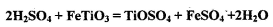
(1)净化钛矿石时,是否需要除去杂质FeO? ______ (填“需要”或“不需要”)。
(2) 净化钛矿石时,需用浓氢氧化钠溶液来处理,写出该过程中发生反应的化学方程式: __________________
II. TiO2可通过下述两种方法制备金属钛:
“方法一”是电解TiO2来获得Th将处理过的TiO2作阴极,石墨为阳极,熔融CaO为电解液,用碳块作电解槽池。
(3)阴极反应的电极反应式为__________________
“方法二”是先将TiO2与 Cl2、C反应得到TiCl4,再用镁还原得到TL因下述反应难于发生: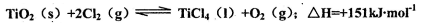
所以不能直接由Ti02和Cl2反应(即氯化反应)来制取TiCl4。当往氯化反应体系中加入碳后,碳与上述反应发生耦合,使得反应在高温条件下能顺利进行。
(4) 己知:
请写出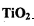 与Cl2、C反应制取TiO4的热化学方程式:____________
与Cl2、C反应制取TiO4的热化学方程式:____________
(5)从化学平衡的角度解释:往氯化反应体系中加入碳时,氯化反应能顺利进行的原因________________________________________________
查看答案和解析>>
科目:高中化学 来源:2011-2012学年四川省自贡市高三上学期第一次诊断性考试理综试题(化学部分) 题型:实验题
(14分) 在工业生产和日常生活中有重要用途。 I.工业上用钛矿石(
在工业生产和日常生活中有重要用途。 I.工业上用钛矿石( ,含
,含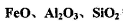 等杂质)经过下述反应制得:
等杂质)经过下述反应制得:

其中,步骤②发生的反应为:
(1)净化钛矿石时,是否需要除去杂质FeO? ______ (填“需要”或“不需要”)。
(2) 净化钛矿石时,需用浓氢氧化钠溶液来处理,写出该过程中发生反应的化学方程式: __________________
II. TiO2可通过下述两种方法制备金属钛:
“方法一”是电解TiO2来获得Th将处理过的TiO2作阴极,石墨为阳极,熔融CaO为电解液,用碳块作电解槽池。
(3)阴极反应的电极反应式为__________________
“方法二”是先将TiO2与 Cl2、C反应得到TiCl4,再用镁还原得到TL因下述反应难于发生:
所以不能直接由Ti02和Cl2反应(即氯化反应)来制取TiCl4。当往氯化反应体系中加入碳后,碳与上述反应发生耦合,使得反应在高温条件下能顺利进行。
(4) 己知: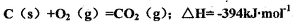
请写出 与Cl2、C反应制取TiO4的热化学方程式:____________
与Cl2、C反应制取TiO4的热化学方程式:____________
(5)从化学平衡的角度解释:往氯化反应体系中加入碳时,氯化反应能顺利进行的原因________________________________________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com